







Spontanität der Reaktionen Die Variation der → Gibbs freien Enthalpie bestimmt, ob eine Reaktion spontan ist oder nicht.
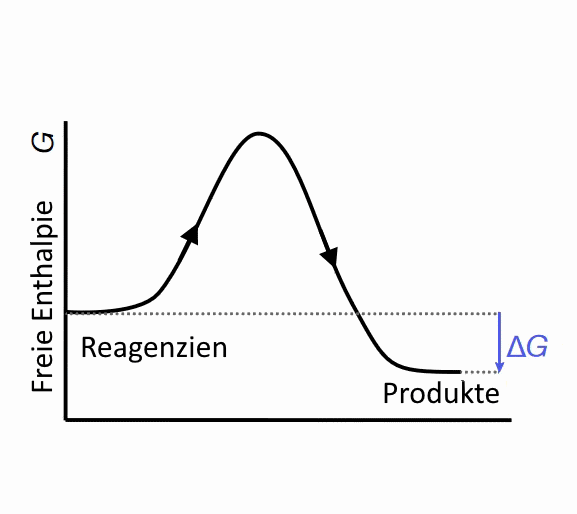
In diesem Fall ist die freie Enthalpiedifferenz von Gibbs $ \Delta \; G $ zwischen Produkten und Reagenzien negativ. Die Reaktion ist spontan, aber das heiÃt nicht, dass sie schnell ist!
Reaktionsgeschwindigkeit, Aktivierungsenergie Die Geschwindigkeit einer spontanen Reaktion hängt im Wesentlichen von der Höhe der Aktivierungsenergiebarriere zwischen Reagenzien und Produkten ab.
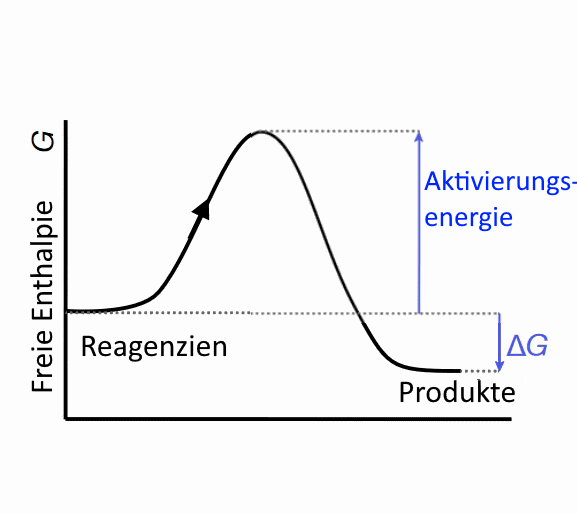
Diese Barriere beruht auf der Tatsache, dass eine Reaktion häufig durch energetisch ungünstige Zwischenprodukte verlaufen muss:
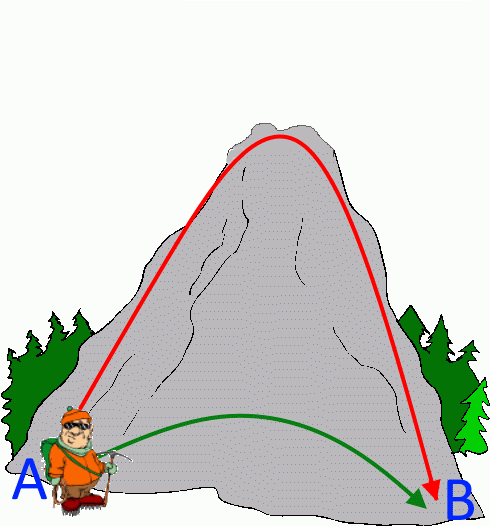
Um von A nach B zu gelangen, hat Pompommymountain jedes Interesse daran, den Greenway zu nehmen: Es ist schneller und er wird genauso viel Energie gewinnen wie der Rote!
Katalysatoren Ein Katalysator reduziert die Aktivierungsenergie, indem er weniger energetische Zwischenprodukte bereitstellt.
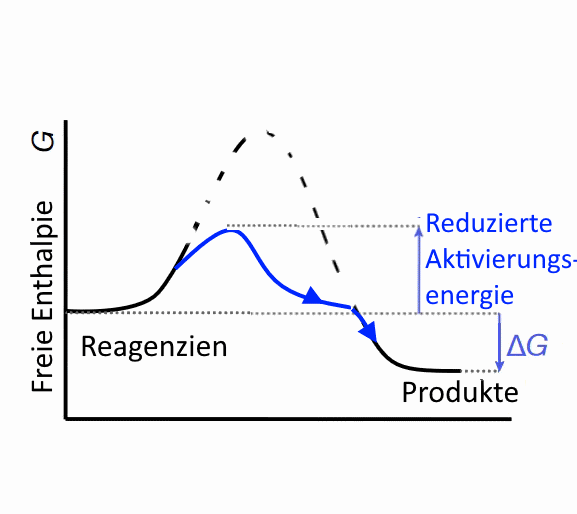
Der Katalysator beschleunigt somit die chemische Reaktion. Ein einfaches Beispiel findet man → hier . In der Biochemie werden die Katalysatoren Enzyme genannt.
Lactose Laktose ist ein Dimer von $ \beta $ -Galaktose und $ \beta $ - Glukose . Dies ist der Hauptzucker der Milch. Im Darm wird seine Hydrolyse durch das Enzym Lactase katalysiert. Dies ist der erste Schritt in seiner Verdauung.
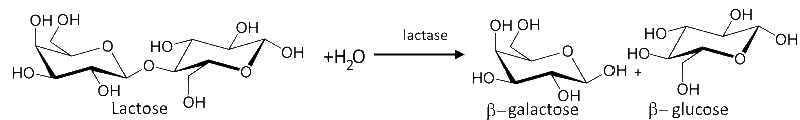
Lactase Das Enzym Lactase (eine $\beta $ - Galactoxidase) ist ein hochkomplexes Polypeptid mit einer Molmasse von mehr als 15000:
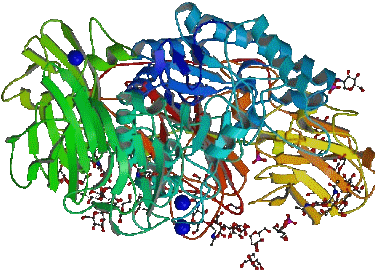
Die farbigen Banden repräsentieren Polypeptidketten.
Laktoseintoleranz Ein Mangel an Laktase (Ursachen: Genetik, Darmverletzung oder anscheinend ein zu privatives vorheriges Regime bei Milchprodukten) führt zu einer Unverträglichkeit, die sich in Durchfall, Krämpfen, Erbrechen, Gasen äuÃert.