







Ist der pH-Wert des Mediums niedrig ([H_3O^+] $ hoch), wird das Carboxylat zu einer neutralen Carboxylgruppe, das Ammoniumion bleibt in der positiven Form:

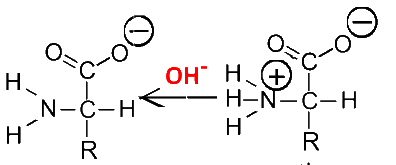
Andererseits ist der pH-Wert des Mediums hoch ($ [OH^-] $ hoch),verwandelt sich das Ammoniumion in eine neutrale Aminogruppe, das Carboxylation bleibt in negativer Form:
Gleiches gilt für Ammonium- oder Carboxylatgruppen in den Seitenketten, zum Beispiel:

Wir sehen, dass die Gesamtladung der Aminosäure vom pH-Wert des Mediums sowie von den in der Seitenkette vorhandenen Funktionen abhängt: - Bei einem niedrigen pH-Wert und einer Seitenkette, die bereits "sauer" ist (Vorhandensein einer Carbonsäurefunktion), ist die Aminosäure global positiv geladen. - Bei einem niedrigen pH-Wert und einer bereits "basischen" Seitenkette (Vorhandensein einer Aminfunktion oder dergleichen) ist die Aminosäure im allgemeinen negativ geladen. - Bei einem pH-Wert von ca. 7 und einer neutralen Seitenkette ist die Aminosäure im Allgemeinen neutral.
Wir nennen isoelektrischer Punkt ($ pI $) den $ pH $, an dem die Aminosäure global neutral ist. - Für basische Aminosäuren ("basische" Seitenkette) $ pI \ca. $ 9,5 - Für saure Aminosäuren (Seitenketten- "Säure") $ pI \ca. 3 $ - Für neutrale Aminosäuren (mit "neutraler" Seitenkette) $ pI \ca. $ 6
Wenn die Aminosäureseitenkette nur $ C $ - oder $ H $ - Atome enthält, ist der Unterschied → der Elektronegativität schwach, Wechselwirkungen der Art Van der Waals zwischen diesen Seitenketten sind sehr schwach :

Wenn die Seitenkette der Aminosäuren starke polare Gruppen aufweist ($ O-H $, $ -NH_2 $ ...), kann die → Dipol-Dipol oder → H-Bindung zwischen diesen Seitenketten sehr stark sein:

Unpolare Aminosäuren haben niedrige unpolare Seitenketten. Polare Aminosäuren haben starke polare Seitenketten.
Lysin ist .......... Valin ist .......... Serin ist .......... Asparaginsäure ist ..........