Säure-Base Titrierung
Tutorial 3



 pH-Wert beim Titrieren einer starken Base mit einer starken Säure
Schema
pH-Wert beim Titrieren einer starken Base mit einer starken Säure
Schema
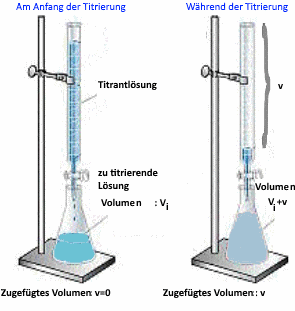
Bestimmung des Volumens $ V_e $ der am äquivalenten Punkt (P.E.) zugegebenen Säure
Am P.E.:
$n_{hinzugefügte\; Säure}= n_{Base am Anfang}$
$V_e\cdot c_{Säure}=V_i\cdot c_{Base}$
und so kriegt man $V_e$
pH-Wert je nach Volumen $ v $ zugegebener Säure
$v=0$
pH einer starke Base von der Molarität $c_{Base}$:
$pH=14+logc_{Base}$
$v\lt V_e$
Bestimmen der Anzahl der Mole Base $ n_b $, die noch nicht reagiert haben
$pH=14+log\frac{n_b}{V_i+v}$
$v\;=\;V_e$
$pH=7$
$v\gt V_e$
Bestimmen der Anzahl der Mole Säure $ n_a $ im Ãberschuss
$pH=-log\frac{n_a}{V_i+v} $
$20\;mL\; NaOH \;0,10 \;M$ werden mit $HCl\;0,1\;M$ titriert. Berechnen Sie den pH-Wert zu Beginn der Titration.
Für Antworten verwenden Sie die Pfeile ↑ und ↓ oben!
Beenden Sie bitte diese Frage, bevor Sie zur nächsten übergehen!
Starke Base:
$pH$ $=$ $14+log\;c_{Base}$
$pH$ $=$ $14$ $+$ $log\;0,10$ $=$ $13$



