Reaktion zwischen konzentrierter Salpetersäure und Kupfer

Der Becher ist mit einer konzentrierten Salpetersäurelösung gefüllt, das rote Metall ist Kupfer. Im Becherglas ist ein umgekippter Trichter, der in ein kleines Reagenzglas hineinleitet.
Das Kupfer wird am Boden des Bechers eingeführt.
Jetzt befindet sich das Stuck Kupfer unter dem Trichter.
Eine chemische Reaktion wird ausgelöst. Die Farbe zeigt die Bildung des Kupfer(II)-Ions an.
Ein farbloses Gas bildet sich. Es ist Stickstoffmonoxid.
Der Trichter leitet das Gas zum Reagenzglas.
Stickstoffmonoxid wird in dem Reagenzglas gesammelt.
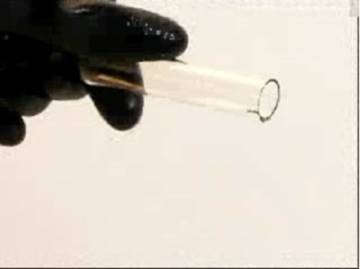
Wir nehmen das Reagenzglas raus.
Stickstoffmonoxid (farblos) wird mit Luft in Kontakt gebracht.
In Kontakt mit dem Sauerstoff der Luft bildet sich ein braunes Gas : Es ist Stickstoffdioxid.









Der Becher ist mit einer konzentrierten Salpetersäurelösung gefüllt, das rote Metall ist Kupfer. Im Becherglas ist ein umgekippter Trichter, der in ein kleines Reagenzglas hineinleitet.

Kommt aus der Seite Educnet


















