







Si le $pH$ du milieu est faible ( $[H_3O^+]$ élevée), l'ion carboxylate se transforme en groupe carboxyle neutre, l'ion ammonium reste sous forme positive:

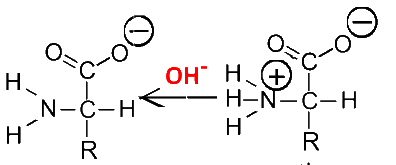
Par contre, si le $pH$ du milieu est élevé ( $[OH^-]$ élevée), l'ion ammonium se transforme en groupe amine neutre, l'ion carboxylate reste sous forme négative:
Il en est de même pour des groupes ammonium ou carboxylate se trouvant dans les chaînes latérales, p. exemple:

Wir sehen, dass die Gesamtladung der Aminosäure vom pH-Wert des Mediums sowie von den in der Seitenkette vorhandenen Funktionen abhängt: - Bei einem niedrigen pH-Wert und einer Seitenkette, die bereits "sauer" ist (Vorhandensein einer Carbonsäurefunktion), ist die Aminosäure global positiv geladen. - Bei einem niedrigen pH-Wert und einer bereits "basischen" Seitenkette (Vorhandensein einer Aminfunktion oder dergleichen) ist die Aminosäure im allgemeinen negativ geladen. - Bei einem pH-Wert von ca. 7 und einer neutralen Seitenkette ist die Aminosäure im Allgemeinen neutral.
Wir nennen isoelektrischer Punkt ($ pI $) den $ pH $, an dem die Aminosäure global neutral ist. - Für basische Aminosäuren ("basische" Seitenkette) $ pI \ca. $ 9,5 - Für saure Aminosäuren (Seitenketten- "Säure") $ pI \ca. 3 $ - Für neutrale Aminosäuren (mit "neutraler" Seitenkette) $ pI \ca. $ 6
Si la chaîne latérale des acides aminés ne comporte que des atomes $C$ ou $H$, dont la différence d'→ électronégativité est faible, les interactions du type de → Van der Waals entre ces chaînes latérales sont très faibles:

Si la chaîne latérale des acides aminés comporte des groupes fortement polaires, ($O-H$, $-NH_2$...), dont la différence → dipôle-dipôle ou le → pont H entre ces chaînes latérales peuvent être très fortes:

- Les acides aminés non polaires ont des chaînes latérales non polaires dont l'interaction est faible. - Les acides aminés polaires ont des chaînes latérales polaires dont l'nteraction est forte.
La lysine est .......... La valine est .......... La sérine est .......... L'acide aspartique est ..........