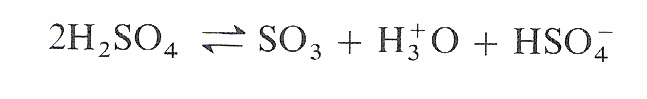- Hückel-Regel: Die aromatischen Systeme mit 2n + 2 π Elektronen sind besonders stabil. Mit 2·1 + 2 = 6 πElektronen fällt Benzol unter ese Regel.
- Mit X+ bezeichnen wir ein Reagens, das einen elektrophilen Angriff durchführen kann.
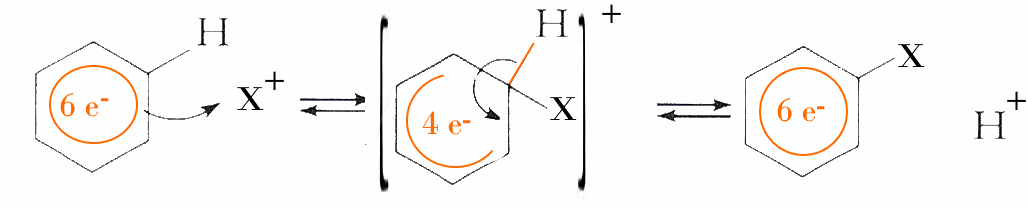 - Der Angriff entfernt 2 Elektronen aus dem aromatischen System, Hückels Regel ist nicht mehr bestätigt: Stabilität ist gefährdet.
- Durch Abspaltung von H+ werden dem aromatischen System 2 Elektronen hinzugefügt: Das substituierte Derivat hat seine Stabilität wiedererlangt!
- Der Angriff entfernt 2 Elektronen aus dem aromatischen System, Hückels Regel ist nicht mehr bestätigt: Stabilität ist gefährdet.
- Durch Abspaltung von H+ werden dem aromatischen System 2 Elektronen hinzugefügt: Das substituierte Derivat hat seine Stabilität wiedererlangt!
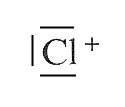 Bildung: Chlor und Aluminiumchlorid
Bildung: Chlor und Aluminiumchlorid
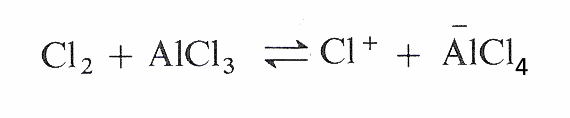
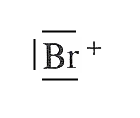 Bildung: Brom und Eisen(III)bromid
Bildung: Brom und Eisen(III)bromid
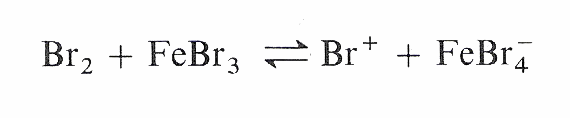
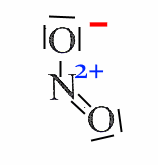 Bildung: Konz. Salpetersäure und konz. Schwefelsäure
Bildung: Konz. Salpetersäure und konz. Schwefelsäure
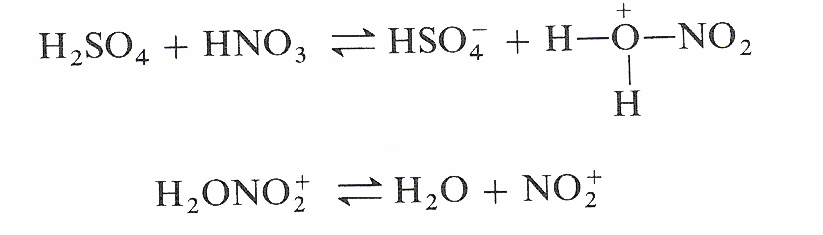
 Bildung: Chloroalkan (oder Säurechlorid) und Aluminiumchlorid
Bildung: Chloroalkan (oder Säurechlorid) und Aluminiumchlorid
 Hier ist R+ = CH3CH2(Ethylium)
Hier ist R+ = CH3CH2(Ethylium)
 Bildung: In der rauchenden Schwefelsäure (Oleum)
Bildung: In der rauchenden Schwefelsäure (Oleum)