Konzentrationen, Dichte, Massendichte,%, Molarität, Massenkonzentration
Tutorial 8

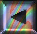
Benützen Sie bitte das folgende schematische "Gitter" und → die Definitionen um die folgende zu lösen:

Ãbung
Berechnen Sie das Volumen einer $ 32,14 \% $ Salzsäurelösung ($ d = 1,16 $), die aus $20,0 \; mol$ reiner Säure (Salzsäuregas) hergestellt werden kann..
Lösung (bitte klicken):
Schema und Formel:
..........
Berechnung:
..........$m_{so}=n_{so}\cdot M{so}$ $=$ $20.0\cdot 36.5=730\;g$
because $M_{so}=M_{HCL}=36.5\frac{g}{mol}$
$m_{S}$ $=$ $\frac{m_{so}\cdot 100}{\%_{so}}$ = $\frac{730\cdot 100}{32.14}$ = $2271 \; g$
$\rho_S$ = $d_S\cdot 1.0\frac{g}{mL}=1.16\frac{g}{mL}$
$V_S=\frac{m_S}{\rho_S}$ =$\frac{2271}{1.16}=1958\;mL$