







Suche:
Alkane sind Verbindungen von Kohlenstoff- und Wasserstoffatomen, die durch Einfachbindungen miteinander verbunden sind.
Die → Die Hybridisierung von Orbitalen des Kohlenstoffatoms erklärt die Geometrie von Alkanmolekülen:

Diese Werte sind ungefähr in allen Alkanen zu finden.
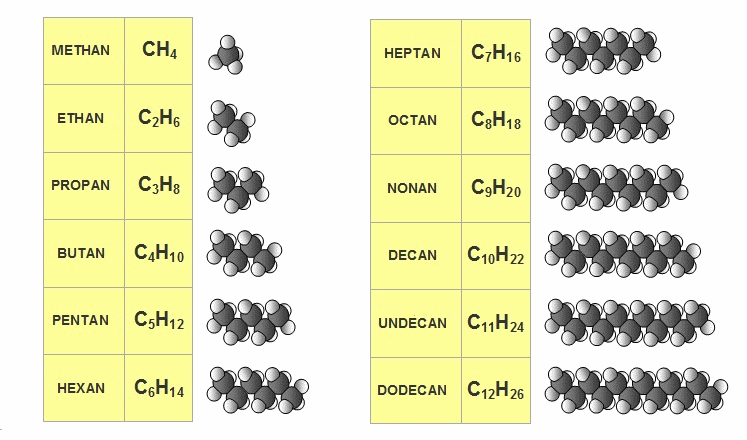
Allgemeine Formel: CnH2n+2 for n=1,2....
Methan, Ethan, Propan und Butan sind bei Raumtemperatur farblose Gase. Die anderen Alkane sind farblose Flüssigkeiten, deren Viskosität mit der Molmasse bis zum Festwerden ansteigt, z.B.

Propanflasche

Hexan
Siedepunkte (teb) und Schmelzpunkte (tfus) nehmen mit der Anzahl n der Kohlenstoffatome zu
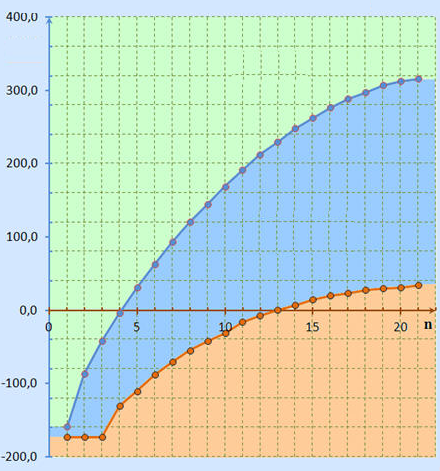
das weil - Je schwerer die Moleküle sind, desto inerter sind sie und desto schwieriger ist es, sie zu trennen und in die Gasphase zu projizieren. - Van-der-Waals-Anziehungskräfte zwischen Molekülen nehmen mit ihrer Kontaktfläche zu
Alkane sind unlöslich im Wasser weil

- sie sind unpolare Moleküle, da der Elektronegativitätsunterschied zwischen Kohlenstoff (2.5) und Wasserstoff (2.1) gering ist - Wasser ist polar und wir wissen, dass sich polare und unpolare Moleküle nicht vermischen (siehe hier ).
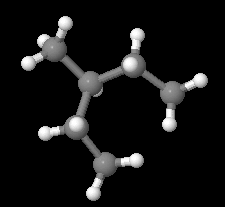
3-Methylpentan
Allgemeine Formel: CnH2n+2 for n=1,2....
Nomenklatur wird → hier erklärt Andere Beispiele können → hier gefunden werden

Cyclopentan
Allgemeine Formel: CnH2n for n=1,2....
Andere Beispiele können → hier gefunden werden
Verzweigte Alkane haben im Allgemeinen Siedepunkte (teb) und Schmelzpunkte (tfus) , die kleiner als die von linearen Alkanen mit der gleichen Anzahl von Kohlenstoffatomen sind , zum Beispiel:
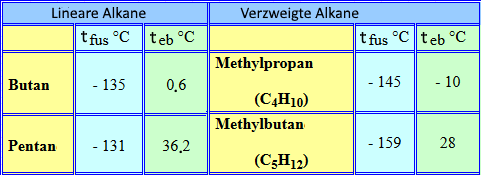
Dies liegt daran, dass diese Moleküle eine kleinere Kontaktfläche zwischen sich haben, also schwächere intermolekulare Kräfte! Solche Substanzen sind wie lineare Alkane wasserunlöslich und aus demselben Grund.
Die cyclischen Alkane haben im Allgemeinen Siedepunkte (teb) und Schmelzpunkte (tfus), die denen von linearen Alkanen mit der gleichen Anzahl von Kohlenstoffatomen überlegen sind, Beispiel:
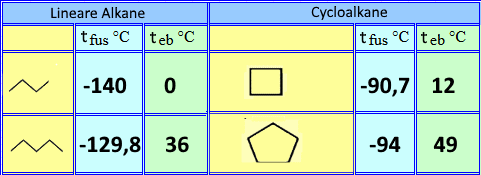
Dies liegt daran, dass diese Moleküle aufgrund ihrer Regelmäßigkeit enger ineinander eingepfercht sind und somit stärkere intermolekulare Kräfte zwischen sich haben! Solche Substanzen sind wie lineare Alkane wasserunlöslich und aus demselben Grund.