Säure-Base Titrierung
Tutorial 15



 pH-Wert beim Titrieren einer schwachen Säure mit einer starken Base
Schema
pH-Wert beim Titrieren einer schwachen Säure mit einer starken Base
Schema
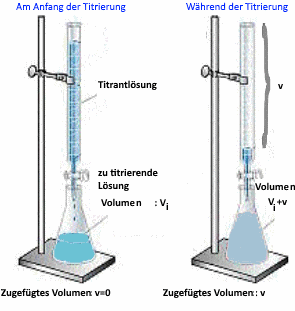
Bestimmung des Basenvolumens $ V_e $, das am äquivalenten Punkt (P.E.) hinzugefügt wird
Zum P.E.:
$ n_{hinzugefügte\; Base } = n_{Säure \; am \; Anfang} $
$ V_e \cdot c_{Base} = V_i \cdot c_{Säure} $
daher $ V_e $
pH basierend auf dem hinzugefügten $ v $ Basenvolumen
$ v = 0 $
pH-Wert einer schwachen Säure der Molarität $ c_{Säure} $:
$x=[H_3O^+]$
$x^2+c_{Säure}x-c_{Säure}K_a=0$
etc ..
$ v \lt V_e $
Bestimmen Sie die Anzahl der Mole der schwachen Säure $ n_a $, die noch nicht reagiert haben, und die Anzahl der Mole der gebildeten Base $ n_b $.
pH-Wert eines Puffers
$pH=pK_a+log\frac{n_b}{n_a}$
$ v = V_e $
pH-Wert einer schwachen Base der Molarität $ c_b $:
Die Molzahl der zu diesem Zeitpunkt vorhandenen schwachen Base ist $ n_b $ $ = $ $ n_ {hinzugefügte\; Base } $ $ = $ $ n_ {Säure \; am \; Anfang} $
Dann gilt: $ c_b = \frac{n_b}{V_i + V_e} $
dann
$ x = [OH^-] $:
$ x^2 + c_bx-c_bK_b = 0$
usw ..
$ v \gt V_e $
Bestimmen Sie die Anzahl Mole $ n_b $ der starken Base im Ãberschuss
$ pH = 14 + log \frac{n_b}{V_i + v} $
$20\;mL\; HCOOH \;0,10 \;M$ werden mit $NaOH\;0,1\;M$ titriert.
Berechnen Sie den pH-Wert zu Beginn der Titration !
$ HCOOH $ ist welche Art von Säure ?
Für Antworten verwenden Sie die Pfeile ↑ und ↓ oben!
Beenden Sie bitte diese Frage, bevor Sie zur nächsten übergehen!
Berechnen Sie $[H_3O^+]$ durch eine Gleichung zweiten Grades !
Es sei $x$ $=$ $H_3O^+$
$x^2+c_ax-c_aK_a$ $=$ $0$
$x^2+0,10\cdot x-0,10\cdot 10^{3,75}$ $=$ $0$
$x=4,27\cdot 10^{-3}\;M$
Berechnen Sie dann den pH-Wert !
$pH$ $=$ $-log[H_3O^+]$ $=$ $-log(4,27\cdot 10^{-3})$ $=$ $2,37$



