Concentrations: molalitûˋ et fraction molaire
Solutûˋ, solvant et solution
Le solutûˋ ($so$) est l'espû´ce dissoute, le solvant (sl) est le liquide dans lequel cette espû´ce est dissoute et la solution (S) est le mûˋlange des deux. La masse de la solution est toujours ûˋgale û la masse du solvant + la masse du solutûˋ.
$m_S$=$m_{so}+m_{sl}$
Une telle ûˋgalitûˋ n'est pas toujours vraie pour les volumes !!
Fraction molaire du solutûˋ ($X_{so}$)
La fraction molaire du solutûˋ est le rapport du nombre de moles de solutûˋ par le nombre de moles total du mûˋlange. Dans le cas d'un seul solutûˋ, le nombre de moles total du mûˋlange est la somme du nombre de moles de soltûˋ et de solvant:
$X_{so}$=$\frac{n_{so}}{n_{so}+n_{sl}}$
Molalitûˋ du solutûˋ ($\mu_{so}$)
La molalitûˋ du solutûˋ est le rapport du nombre de moles de solutûˋ par la masse du solvant.
$\mu_{so}$=$\frac{n_{so}}{m_{sl}}$
si $m_{sl}$ est exprimûˋ en kg
En mettant tout ceci ensemble
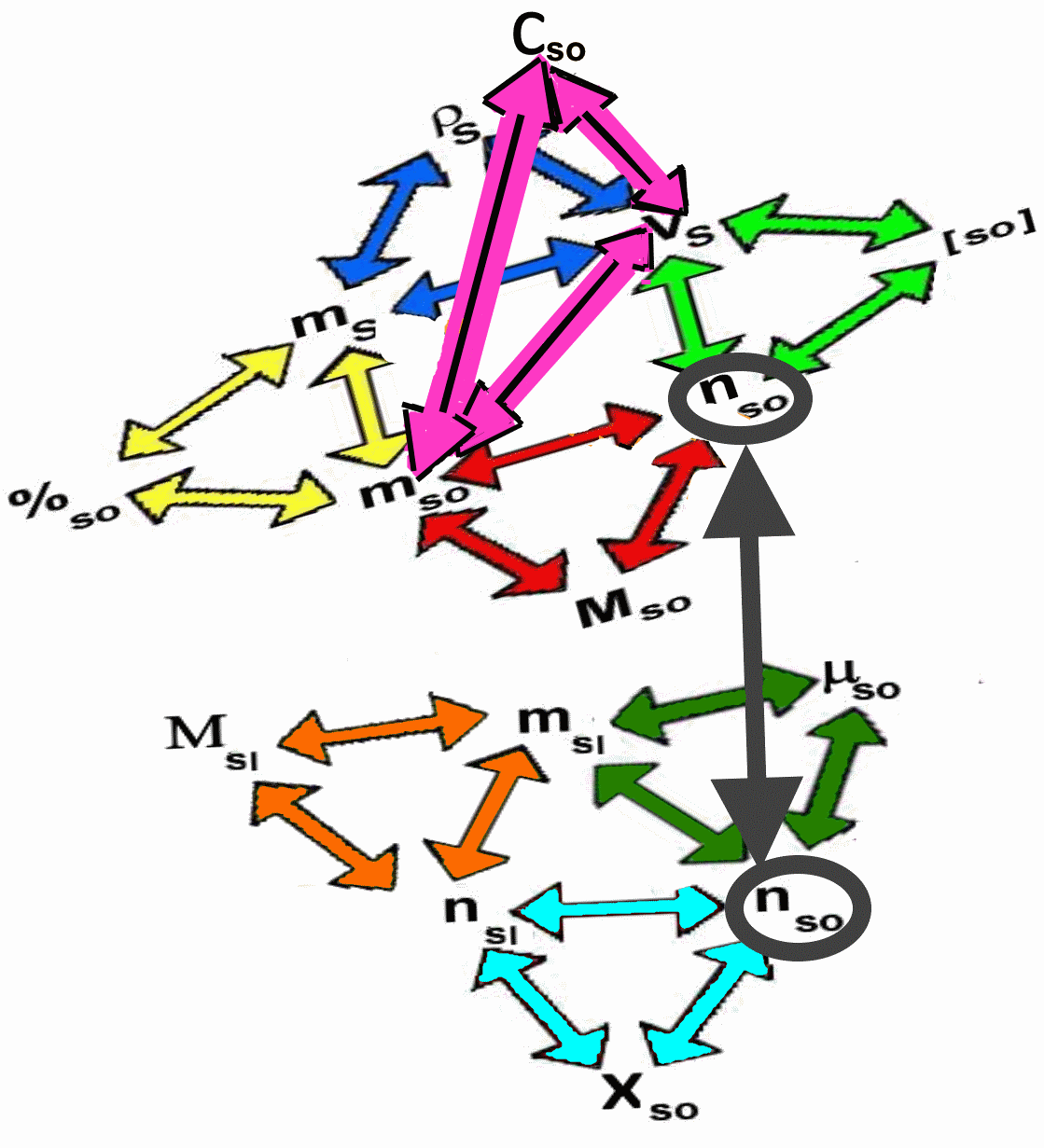
Le treillis
Le treillis suivant rûˋsume les rapports entre les grandeurs prûˋcûˋdentes.
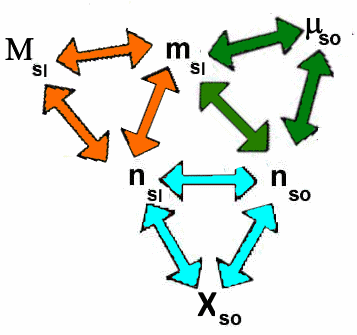
Chaque triangle symbolise une des dûˋfinitions prûˋcûˋdentes. Par exemple, si on connaûÛt $ \mu_{so} $,$n_{so}$, on calcule $m_{sl}$ par le triangle vert, puis $n_{sl}$ par le triangle orange ( connaissant la masse molaire du solvant ), puis encore $X_{so}$ par le triangle bleu!