






La pellicule photographique en matière plastique est recouverte à l'abri de la lumière - à sa face supérieure: 1) d'une émulsion · de gélatine · de bromure de sodium · de nitrate d'argent · de traces de soufre · de traces de sensibilisateurs (colorants semblables au colorant des carottes) 2) d'une couche protectrice de pure gélatine - à sa face inférieure: d'un colorant qui empêche la réflexion de la lumière
Dans l'émulsion, il y a réaction entre le nitrate d'argent et le bromure de sodium: $Ag^+$ $+$ $NO_3^-$ $+$ $Na^+$ $+$ $Br^-$ $\longrightarrow$ $Ag^+Br^-$ $+$ $Na^+$ $+$ $NO_3^-$ Le bromure d'argent précipite sous forme de microcristaux.

Les ions $Ag^+$ et $Br^-$ s'arrangent dans ces cristaux sous forme de réseaux cubiques à face centrée mais présentant des lacunes irrégulières:

Dans ces lacunes quelques ions $Ag^+$ peuvent circuler assez librement:

Quand un photon frappe contre un ion bromure, un électron de valence de celui-ci est excité.
$Br^-$ $+$ $h\nu $ $\longrightarrow $ $Br\cdot$ $ +$ $e^-$
Il se forme un atome de brome.

Mais les photons de la lumière visible n'ont pas assez d'énergie pour transférer cet électron sur un atome d'argent!

Les sensibilateurs absorbent aussi de la lumière et peuvent transmettre ce gain d'énergie à l'électron excité pour le porter dans un niveau quantique ("bande de conduction") où il peut circuler librement dans le cristal et atteindre les ions argent pour les réduire:
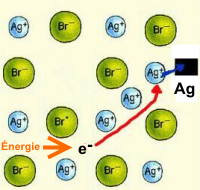
$Ag^+$ $+$ $e^-$ $\longrightarrow$ $Ag$
Les quelques atomes d'argent formés circulant dans le cristal ont tendance à s'agglutiner en surface en gagnant de l'énergie réticulaire (énergie provenant de la formation de la liaison métallique). On a trouvé que ces germes se forment préférentiellement aux endroits où des impuretés comme le soufre constituent des noyaux de condensation. Les germes sont extrêment petits. On ne peut pas les voir à l'oeil nu. On dit qu'ils forment l'image latente.

Une fois exposé, le film est traité dans la chambre noire:
La révélation consiste à former autour des germes une grande quantité d'atomes d'argent afin de réaliser une image réelle:

Pour cela le film est introduit dans un bain constitué de - d'hydroquinone (le révélateur) - de carbonate de sodium - de bromure de potassium (peu) L'hydroquinone

est un réducteur Les systèmes d'oxydo-réduction sont les suivants: (1)

(2)

avec les potentiels standard d'oxydo-réduction suivants:
$E^o_1=0,80\; V$
$E^o_2=0,69\; V$
Nous nous trouvons ici loin des conditions standard, de telle manière qu'il faut considérer la → loi de Nernst:
(a)
$E_1$ $=$ $E^o_1$ $+$ $\frac{0,059}{1}log[Ag^+]$
(b)
$E_2$ $=$ $E^o_2$ $+$ $\frac{0,059}{2}log\frac{[X][H^+]^2}{[H_2X]}$
Du fait de la solubilité très faible du bromure d'argent, $log[Ag^+]$ devient négatif et le potentiel réel $E_1$ du système (a) est considérablement diminué.
L'ajoute des ions carbonate basiques diminue $[H^+]$:
$CO_3^{2-}$ $+$ $H^+$ $\longrightarrow$ $ HCO_3^-$
et abaisse ainsi le potentiel $E_2$ du système (b) en-dessous de $E_1$ !
Alors l'hydroquinone peut réduire les ions argent en atomes d'argent:
$2Ag^+$ $+$ $2e^-$ $\longrightarrow$ $2Ag$
$C_6H_4(OH)_2$ $+$ $2OH^-$ $-$ $2e^-$ $\longrightarrow$ $C_6H_4O_2$ $+$ $2H_2O$
 $2Ag^+$ $+$ $C_6H_4(OH)_2$ $+$ $2OH^-$ $\longrightarrow$ $C_6H_4O_2$ $+$ $2H_2O$
Ion argent + hydroquinone donnent quinone et atome d'argent
$2Ag^+$ $+$ $C_6H_4(OH)_2$ $+$ $2OH^-$ $\longrightarrow$ $C_6H_4O_2$ $+$ $2H_2O$
Ion argent + hydroquinone donnent quinone et atome d'argent
Les ions $Ag^+$ libres qui subsistent dans l'émulsion peuvent provoquer un voile gris ($Ag$ )quand ils sont exposés à la lumière. Le bromure de potassium diminue leur molarité et empêche l'apparition du voile. En effet: $[Ag^+][Br^-]=K_s$ où $K_s$ est le produit de solubilité du bromure d'argent. Si $[Br-]$ augmente par suite de l'addition du bromure de potassium, $[Ag^+]$ doit diminuer.
Si l'hydroquinone agit trop longtemps, la photo risque de devenir trop sombre. On arrête son action après un temps déterminé en acidifiant le milieu et en élevant ainsi son potentiel d'oxydo-réduction (voir en haut). Pour cela le film est introduit dans un bain constitué d'une solution diluée d'acide acétique
Le bromure d'argent qui n'a pas été transformé en argent risque de noircir quand la photo est sortie de la chambre noire. On l'élimine en le complexant par l'ion thiosulfate $S_2O_3^{2-}$. Pour cela le film est introduit dans un bain fixateur constitué d'une solution diluée de thiosulfate de sodium.
$Ag^+Br^-$ $+$ $4Na^+$ $+$ $2S_2O_3^{2-}$ $\longrightarrow $ $3Na^+$ $+$ $ [Ag(S_2O_3)_2]^{3-}$ $+$ $3Na^+$ $+$ $ Br^-$
Le bromure de sodium et le dithiosulfatoargentate de sodium sont solubles dans l'eau et peuvent donc enlevés par lavage
Le développement se termine par un lavage intense à l'eau distillée suivi de séchage.
