







Anker
Ein Copolymer auf Styrolbasis, an das eine Chlormethylgruppe gebunden ist, ist der "Anker", mit dem die Synthese beginnt:
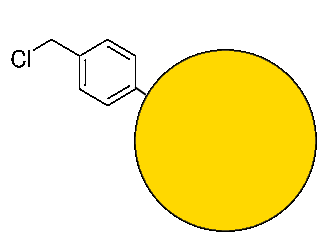
Schutz der ersten Aminosäure
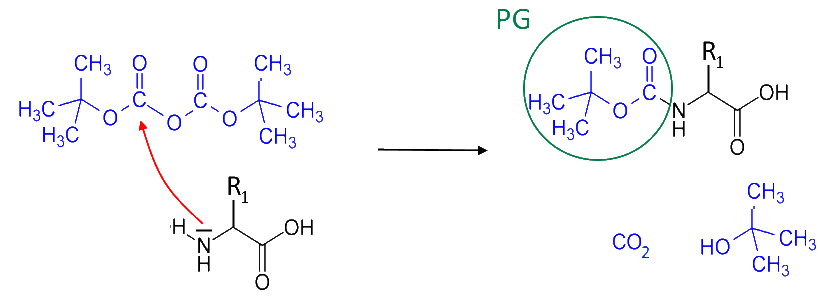
Wir möchten, dass diese Aminosäure nicht mit ihrer Amingruppe $ -NH_2 $ reagiert. Dann wird sie geschützt, indem eine tert-Butyloxycarbonylgruppe (" PG ") durch Reaktion mit dem entsprechenden Säureanhydrid gebunden wird:
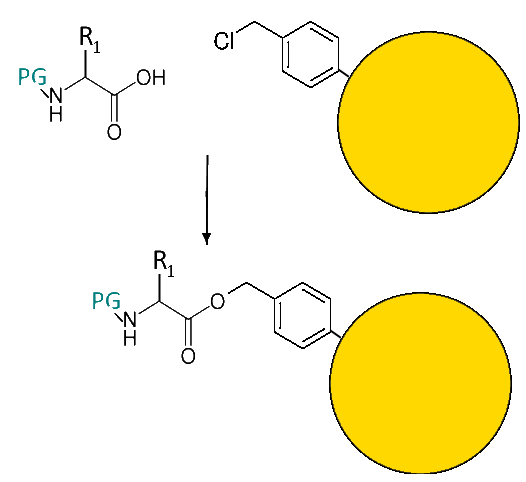
Fixieren der ersten Aminosäure am "Anker":
"Der Anker" und die Carboxylgruppe der ersten Aminosäure sind verestert. Dies ist die einzig mögliche Reaktion, da die Amingruppe blockiert ist!
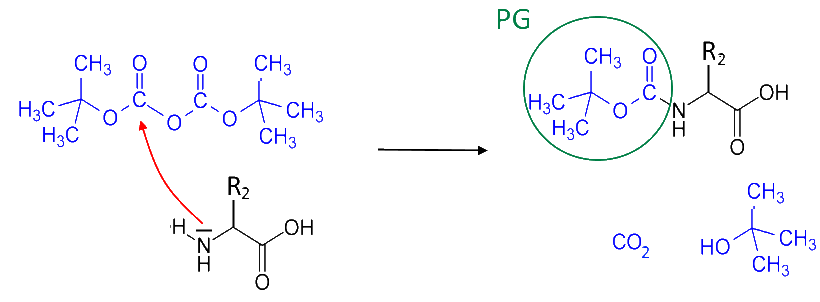
Schutz der zweiten Aminosäure
Eine zweite Aminosäure sieht ihre Amingruppe geschützt:
Entschützen der ersten Aminosäure
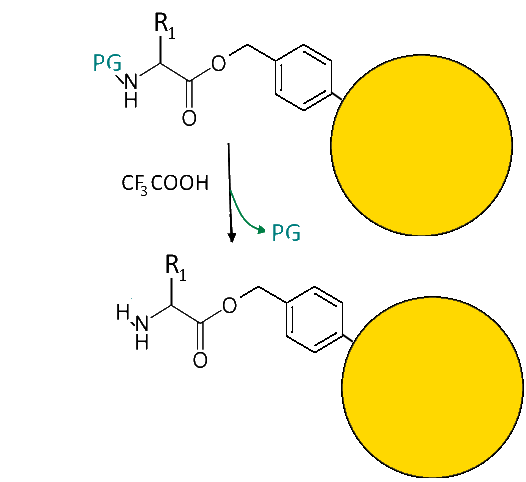
Die Schutzgruppe wird durch Umsetzung mit Trifluoressigsäure von der ersten Aminosäure entfernt:
Peptidbindung
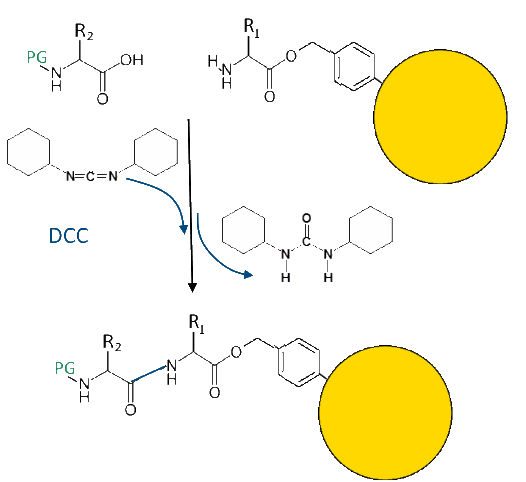
Dicyclohexylcarbodiimid (DCC) stellt die Peptidbindung her, indem es das abgespaltene Wasser fixiert:
Peptidfreisetzung
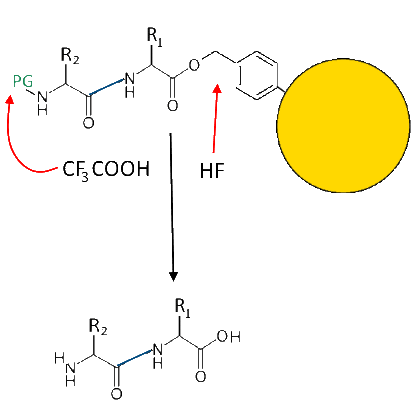
Die Schutzgruppe wird wie oben abgespalten, die Flusssäure bricht die Bindung mit dem Anker und hier ist das Dipeptid!
Diese Methode wurde entwickelt von:

Robert Bruce Merrifield (1921 - 2006)
Es ist ersichtlich, dass das Verfahren verwendet werden kann, um so viele Aminosäuren wie gewünscht zu fixieren, indem die Synthese vor der endgültigen Freisetzung des gewünschten Peptids wiederholt wird! Die Ausbeute ist ausgezeichnet und einige Firmen bieten derzeit die Produktion eines Polypeptids in wenigen Tagen an!