







 | Die gesättigte LuftWenn das Wasser mit Luft in Kontakt kommt, können bewegte Wassermoleküle in die Luft gelangen. So wird unsichtbarer Wasserdampf mit Gasen vermischt, die normalerweise in der Luft vorhanden sind. Luft soll "feucht" werden. Wir spüren diese Feuchtigkeit besonders im Sommer, bei "schwerem" und stürmischem Wetter. In ähnlicher Weise können einige Wassermoleküle, die Wasserdampf bilden, ihre kinetische Energie durch die Gefahr von StöÃen mit anderen in der Luft vorhandenen Molekülen verlieren. Sie verbinden sich mit dem flüssigen Wasser, das mit der Luft in Kontakt steht. Wenn dieser Austausch lange genug andauert, stellt sich ein heterogenes Wassergleichgewicht zwischen der "flüssigen Wasser" -Phase und der "Luft" -Phase ein. Die Luft soll gesättigt sein und wir haben: $K\;=\;\frac{[H_2O]_{Luft}}{[H_2O]_{Wasser}}$ avec: $[H_2O]_{Wasser}\;\approx\;55.6\frac{mol}{L}$ Tatsächlich hat 1 Liter Wasser eine Masse von ungefähr 1000 g und enthält somit ungefähr 18 g = 55,6 mol . Wir finden also: Im Gleichgewicht (gesättigte Luft): $[H_2O]_{Luft}\;=\;K_1$ Wie jede Gleichgewichtskonstante hängt $ K_1 $ von der Temperatur ab. Bei höheren Temperaturen sind die Moleküle bewegter und es ist leicht zu verstehen, dass sich dann mehr Wassermoleküle im Dampfzustand befinden: $ K_1 $ steigt mit der Temperatur. |
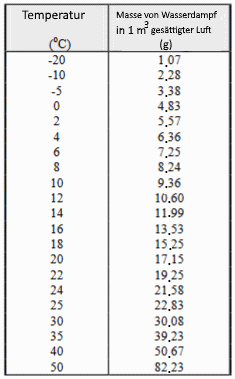
Beispiel: Bei $ 20^oC $ ist die Konstante $ K_1 $ gleich ..........
Das Sättigungsgleichgewicht hat häufig keine Zeit um sich herzustellen und daher bleibt die Konzentration des Wasserdampfs in der Luft geringer als die Konzentration, die dieselbe Luft im Gleichgewicht enthalten könnte. Die relative Luftfeuchtigkeit wird relativ zur (maximalen) Wasserdampfkonzentration in der gesättigten Luft gemessen. Beispiel 1: Eine relative Luftfeuchtigkeit von $ 35\% $ bei $ 30^oC $ bedeutet, dass in einem Liter Luft enthalten ist .......... Beispiel 2: Luft bei $ 40^oC$ mit $ 2,18 \frac{mol}{m^3} \; H_2O $ hat eine relative Luftfeuchtigkeit von ..........
Wenn sich die feuchte und heiÃe Luft abkühlt, kann ihre Wasserdampfkonzentration den Wert von $ K_1 $ bald überschreiten ($ K_1 $ nimmt mit der Temperatur ab). Wenn Kondensationskerne vorhanden sind (bereits vorhandenes Wasser, Staub, Ionen ...), bildet der überschüssige Dampf um diese Kerne herum flüssiges Wasser. Beispiel: $ 1\;m^3$ Luft mit $ 90\% $ Luftfeuchtigkeit kühlt bei konstantem Druck von $ 40^oC $ auf $ 10^oC $ ab. Berechnung: Die Anzahl der Mole Wasserdampf am Anfang: .......... Das Endvolumen (Gay-Lussac-Gesetz): .......... Die Anzahl der Mol, die das Endvolumen maximal enthalten kann: .......... Die Anzahl der Mole und die Kondenswassermasse: ..........
Nasse Luftmassen, die sich abkühlen (aufwärts gerichtete Luft in einem Niederdruckgebiet oder an Hängen eines Gebirges, weniger dichte warme Luft über dichtere kalte Luft in einer störenden feuchten Luft, die sich durch Strahlung abkühlt, in den klaren Herbstnächten kann feuchte Küchenluft, die das kalte Glas berührt, durch Kondensation wasserdampf verlieren, wenn die relative luftfeuchtigkeit von anfang an ausreicht: Wolken, Regen, Nebel oder Kondenswasser bilden sich. Man kann $ 1^oC $ Abkühlung pro $ 100 \; m $ vertikale Distanz zählen, wenn es keine Kondensation gibt, $ 0,5^oC $ pro $ 100 \; m $ im Falle von Kondensation (exotherme Erscheinung).
 .
.
Aufwärtsluft bildet Kumuluswolken
2