





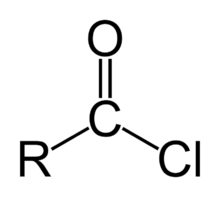
 Säurechlorid
Säurechlorid
- Im Gegensatz zu Carbonsäuren können sie zwischen sich keine Wasserstoffbrückenbindungen bilden. Sie sind daher flüchtiger als die entsprechenden Carbonsäuren. - Bei Kontakt mit Wasser setzen sie $ HCl $ frei, daher ihre tränende Wirkung
Aus einem Video von Franklychemistry

Aus einem Video von Franklychemistry


Die Struktur der funktionellen Gruppe von Säurechloriden erklärt ihre chemische Reaktivität:
- (1) Das Atom $ C $ ist ein elektrophiles Zentrum ($ \delta + $)
Diese Substanzen werden daher nukleophil angegriffen, beispielsweise von $ H_2O^{\delta -} $, $ RO^{\delta -}H $, $ H_3N^{\delta-} $ oder $ RH_2N^{\delta -} $:
Reaktion mit Wasser: $RCOCl + H_2O$ $\rightarrow$ $ RCOOH+ HCl$ Produkt: Die entsprechende Carbonsäure! Reaktion mit einem Alkohol: $RCOCl + R^{'}OH$ $\rightarrow$ $ RCOOR^{'}+ HCl$ Produkt: Der entsprechende Ester! Reaktion mit Ammoniak: $ RCOCl + NH_3 $ $\rightarrow $ $ RCONH_2 + HCl $ Produkt: Das entsprechende nicht N-substituierte Amid! Reaktion mit einem Amin: $ RCOCl + R^{'}NH_2 $ $\rightarrow $ $ RCONHR^{'} + HCl $ Produkt: Das entsprechende N-substituierte Amid!
- (2) Das Einfangen des Atoms $ Cl $ durch ein elektronisches Lücken-Reagenz (z. B. $ AlCl_3 $) hinterlässt eine Ladung $ + $ am $ C $ Atom
Dann können diese Substanzen einen elektrophilen Angriff ausführen, zum Beispiel auf einen Benzolring: Reaktion mit Benzol in Gegenwart von $ AlCl_3 $ (Friedel-Crafts-Reaktion): $ RCOCl + C_6H_6 + AlCl_3 $ \rightarrow $ C_6H_5COR + H^+ AlCl_4^- $ Produkt: Das entsprechende aromatische Carbonylderivat!
Nennen Sie die Endprodukte, die (unter Befolgung der obigen Schritte) von den Reaktanten erhalten wurden: - Methanoylchlorid und Isopropanol →
- Ethanoylchlorid und Methanamin →
- Methanoylchlorid und Benzol (mit $AlCl_3$) →