







Suche:
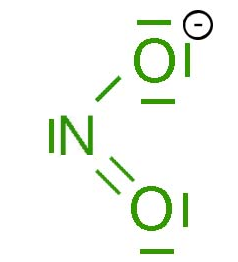
Ausser im Punkt 1, gebrauchen Sie eine verdünnte Lösung von $KNO_2$
|
1. $H_2SO_4$ (eventuell warm) |
Dismutation: $3NO_2^-+2H^+$ $\longrightarrow$ $NO_3^-+2NO+H_2O$ - In der Luft wird $ NO $ zu $ NO_2 $ oxidiert, einem roten Gas! |
|
2. $MnO_4^-$ (Kaliumpermanganat in saurem Medium) |
|
Oxidation ($NO_2^-$ Reduziermittel): $NO_2^-$ $+$ $H_2O$ $-$ $2e^-$ $\longrightarrow$ $NO_3^-$ $+$ $2H^+$/$E_o=0,94V$ $5NO_2^-$ $+$ $2MnO_4^-$ $+$ $6H^+$ $\longrightarrow$ $5NO_3^-$ $+$ $2Mn^{2+}$ $+$ $3H_2O$ |
|
3. $I^-$ (Kaliumiodid in einem sauren Medium) |
|
Reduktion ($NO_2^-$ Oxidiermittel): $NO_2^-$ $+$ $2H^+$ $+$ $e^-$ $\longrightarrow$ $NO$ $+$ $H_2O$/$E_o=0,99V$ $2NO_2^-$ $+$ $4H^+$ $+$ $2I^-$ $\longrightarrow$ $2NO$ $+$ $2H_2O+I_2$ |
|
4. Diphenylamin in Gegenwart von konz. $H_2SO_4$ |
|
Marineblaue Farbe (Befeuchten Sie das Innere eines Reagenzglases mit dem Reaktanten und geben Sie danach ein paar Tropfen Nitrit hinzu.) Diese Reaktion ist sehr empfindlich, aber nicht spezifisch; Nitrate und Chlorate tun dasselbe. |
|
5. Diazotierung (Griessreaktion) |
|
(Mit Nitratspuren arbeiten! In einem Reagenzglas mischen: 1-2 ml einer Essigsäurelösung von Sulfanilsäure mit 1-2 ml einer Essigsäurelösung von α Naphthylamin. Fügen Sie einen Tropfen der verdünnten Nitritlösung hinzu. Es bildet sich eine kirschrote Verbindung. ) - Sehr empfindliche Reaktion - Spezifische Reaktion |