Die scheinbar einfache Reaktion der Zinkkorrosion durch Säure $ Zn + 2H^+ $ $ \rightarrow $ $Zn^{2+} + H_2 $ wirft viele Verständnisprobleme auf: 1) Ist es möglich, dass positive Zn- und H-Ionen kontinuierlich in entgegengesetzte Richtungen diffundieren, die $ Zn^{2+} $ -Ionen vom festen Zink zur Lösung, die $ H^+ $ -Ionen von der Lösung zum festen Zink? Die Physik lehrt uns, dass sich positive Ladungen in einem elektrischen Feld immer in eine Richtung bewegen! 2) Wie kommt es, dass die Reaktion mit unreinem Zink (das Spuren anderer Metalle enthält) viel schneller verläuft als mit hochreinem Zink? 3) Wie kann erklärt werden, dass die Zugabe von etwas Kupfersulfat die Reaktionsgeschwindigkeit (Katalysator) signifikant erhöht? Schauen Sie sich die Oberfläche eines Zinkstücks an, das mit einem Kupferkorn verunreinigt ist (Verunreinigung von Anfang an vorhanden oder durch die Reaktion von $ Cu^{2 +} $ auf $ Zn $ entstanden) und in eine Säurelösung getaucht ist:

Dieses System entspricht einer Batterie:

Tatsächlich wird der Leiter (Kurzschluss!) vom Zink selbst bereitgestellt und das $ Zn^{2+} $ Ion und die $ H_2 $ Moleküle bilden sich unmittelbar nach dem Transfer der ersten Elektronen, wohingegen $ H^+ $ Ionen, abgestoßen durch das $ Zn^{2+} $ -Ion das Zink nicht direkt angreifen können (Rolle der semipermeablen Wand in der Batterie)! Die lokale Batterie funktioniert bis zur Erschöpfung des Zinks oder der $ H^+ $ -Ionen.
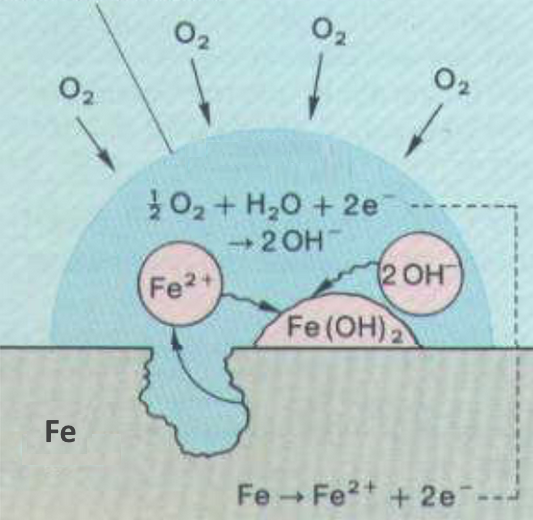
Die Erfahrung zeigt, dass Wasser und Sauerstoff für die Rostbildung notwendig sind. Verunreinigungen in der Luft ($ CO_2 $, $ SO_2 $, Staub) sowie Salze in Wasser fördern den Prozess. Eine lokale Zelle erklärt, was passiert: In sauerstoffarmen Regionen geht Eisen in Form von Eisen(II) -Ionen in Lösung. (Minuselektrode der Batterie). Es verbleiben 2 Elektronen, die im Metallkörper zirkulieren können ("äußerer" Stromkreis der Batterie). Auf der Oberfläche des Eisens nimmt diese an den Stellen, an denen die Lösung sauerstoffreich ist (positive Elektrode der Batterie), mit Hilfe von Wasser Elektronen auf, um Hydroxidionen zu bilden. Eisen(II) -Ionen und Hydroxidionen diffundieren in der Lösung gegeneinander: $ Fe^{2+}(OH^-)_2 $ wird ausgefällt. Dann erzeugt der Sauerstoffüberschuss Rost: $ 4Fe(OH)_2 + O_2 $ $ \rightarrow $ $ 2Fe_2O_3.H_2O + 2H_2O$ Rost (Eisen(II)-oxidhydroxid) ist porös und bewirkt, dass der Prozess bis zum Verschwinden des Eisens fortgesetzt werden kann.