





$ H_2 $ fügt sich einem Alken in Gegenwart von Katalysatoren aus Platin, Palladium oder Nickel/Aluminium-Legierungen hinzu.

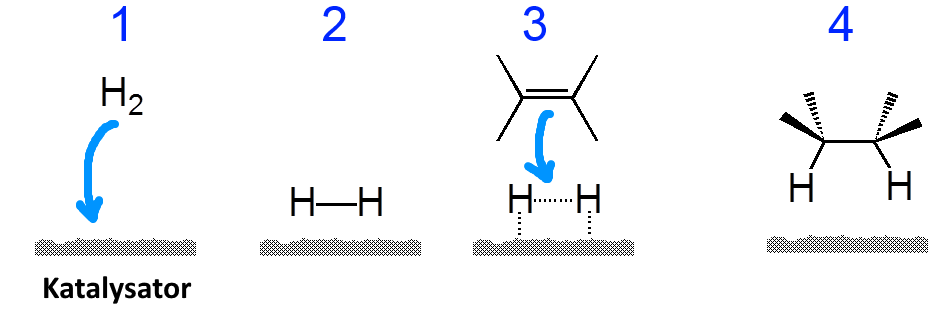
Die Adsorption (1) eines Moleküls $ H_2 $ an einer aktiven Stelle (2) eines dieser Katalysatoren aktiviert das Molekül (3) und erlaubt die Addition (4):
$ HCl, HBr, HI $ addieren sich leicht auf ein Alken, $ HF $ zerstört das Alken

$ H_2O $ addiert sich in saurem Medium bei $ 150^oC $

Diese Zusätze sind stereospezifisch:
Markovnikov-Regel
 $ H $ befindet sich immer an dem am wenigsten substituierten C-Atom der C = C-Bindung
$ H $ befindet sich immer an dem am wenigsten substituierten C-Atom der C = C-Bindung
In Rot der am wenigsten substituierte Kohlenstoff (der die wenigsten Substituenten aufweist, die sich von Wasserstoff unterscheiden):
1)

2)


a) Elektrophiler Angriff auf das π- Dublett b) Einfangen von Chloridionen

(1) ist stabiler als (2), da der induktive Effekt der beiden Methylgruppen das positive Loch "stopft", besser als der Effekt einer Ethylgruppe. (1) hat daher eine längere Lebensdauer, wodurch dem Chlorid mehr Zeit geboten wird um sich zu fixieren.
$Cl_2, Br_2$ addiern sich leicht zu einem Alken, $ F_2 $ zerstört das Alken, $ I_2 $ addiert sich nicht

Video angepasst von Netexperimente (Sven Sommer)

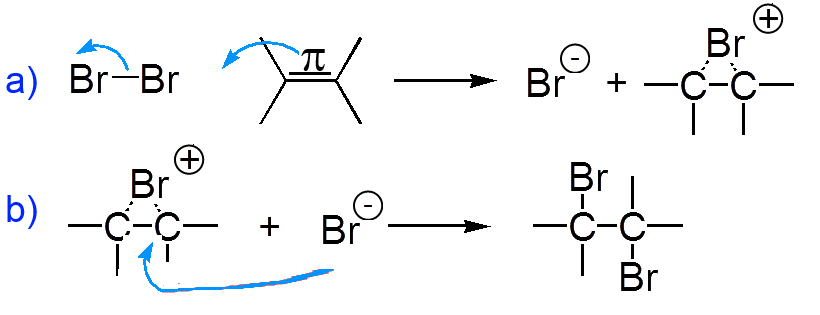
a) Elektrophiler Angriff von Brom (elektronegativ!) auf π - Duplett b) Nucleophiler Angriff des Bromidions "von hinten"
Es wird ein intermediäres Brommoniumion gebildet. Beachten Sie die multizentrische Bindung, die sich nicht an die traditionellen Strukturen von Lewis hält!
Die Reaktion von Ethen mit Brom in Natriumchloridlösung führt sowohl zu 1,2-Dibromethan als auch zu 1-Brom-2-chlorethan.
