






Svante Arrhenius (18591927)
Eine Säure ist eine Substanz , die im Wasser das Wasserstoffion $H^+$ freisetzt Eine Base ist eine Substanz , die im Wasser das Hydroxid-Ion $OH^- $ freisetzt
& nbsp;Salzsäure $HCl$: $HCl$$ \;_\longrightarrow^{Wasser}$ $ H^+$ $ +$ $ Cl^-$ Schwefelsäure $H_2SO_4$: $H_2SO_4 $$\; _\longrightarrow^{Wasser}$ $ H^+$ $+$ $HSO_4^-$ Phosphorsäure $H_3PO_4$: $H_3PO_4$$ \; _\longrightarrow^{Wasser}$ $H^+$ $+$ $HPO_4^{2-}$ Die Base Natriumhydroxid $NaOH$: $NaOH$$\; _\longrightarrow^{Wasser}$ $Na^+$ $+$ $OH^-$ Die Base Kalziumhydroxid $Ca(OH)_2$: $Ca(OH)_2$$\; _\longrightarrow^{Wasser}$ $Ca^{2+}$ $+$ $2OH^-$
Farbige Indikatoren zeigen an, ob eine Lösung sauer, basisch oder neutral ist, z. B. Bromthymol:

in der Mitte 1) Säure 2) neutral 3) basisch
Lassen Sie uns die Wirkung dieses Indikators auf drei Salzlösungen testen, die jeweils zwei Ionenarten enthalten:

Wir können sehen, dass es nicht das Ion $ Cl^- $ ist, das den Säure-Charakter hat, sondern das Ion $ NH_4^+ $. Ebenso hat nicht das Ion $ Na^+ $ den Basecharakter, sondern das Ion $ OH^- $
Die Definition von Säuren und Basen sollte nicht auf Substanzen beschränkt sein, sondern die Ionen enthalten
Die durch die Dissoziation einer Säure in Wasser gebildeten Ionen leiten den elektrischen Strom:
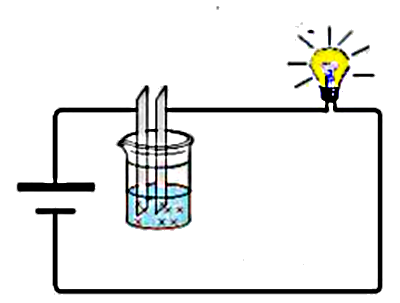
Lassen Sie uns den Einfluss des Lösungsmittels auf diese Dissoziation testen:

Es ist klar, dass Alkohol auch die Dissoziation von Säuren in Ionen ermöglicht!
Die Definition von Säuren und Basen sollte nicht auf das einzige Wasserlösungsmittel beschränkt sein.
Das $H$ -Wasserstoffatom hat ein Proton, das den Kern bildet, und ein Elektron in der Elektronenwolke. Durch Entfernen seines Elektrons wird das Wasserstoffion $H^+ $ erzeugt, das tatsächlich nicht mehr als ein einzelnes Proton ist. Wegen seines extrem kleinen Durchmessers und seiner positiven Ladung muss es eine unwiderstehliche Anziehungskraft auf alle Moleküle ausüben, die ihn umgeben, besonders wenn sie polarisiert sind. !
Das Wasserstoffion kann in einer Lösung nicht allein existieren!
Es war notwendig , die Definition von Arrhenius, zu einfach, auf andere chemische Spezies, andere Lösungsmittel auszudehnen und die Idee eines freien $H^+$ -Ions in Lösung aufzugeben. Dieser Schritt wurde von Johannes Nikolas Brønstedt begangen.