







Sie haben eine $ 0,200 M $ Lösung von $H_3C_6H_5O_7$
(Zitronensäure, $K_a$ $=$ $3.5\cdot 10^{-4}$)
Gleichgewicht der Hydrolyse:
$H_3C_6H_5O_7$ $+$ $H_2O$ $H_3O^+$ $+$ $H_2C_6H_5O_7^-$
$H_3O^+$ $+$ $H_2C_6H_5O_7^-$
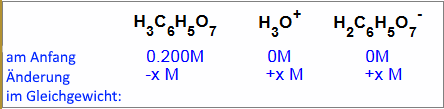
Was sind die Gleichgewichtskonzentrationen jeder Art? Für die Antwort, klicken Sie auf den Pfeil ↓ oben
a) $0,200\;M$, $x\;M$, $(0,200-x)\;M$ b) $0\;M$, $0,200\;M$, $0,200\;M$ c) $(0,200-x)\;M$, $x\;M$, $(0,200+x)\;M$ d) $(0,200-x)\;M$, $x\;M$, $x\;M$
Die Antwort d) ist richtig, $(0.200 - x)\;M$, $0$ $ +$ $ x$ $=$ $x\;M$, $0$ $ +$ $ x$ $=$ $x\;M$.