







Suche:
Alle Atome neigen dazu, sich zu stabilisieren, indem sie die stabile Struktur von Edelgasen einnehmen.
Dies kann zum Beispiel erfolgen
- indem man ein oder mehrere Elektronen gewinnt, um das Oktett der letzten Schicht zu vervollständigen:

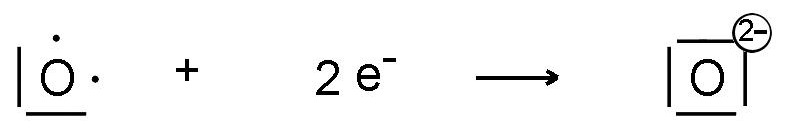
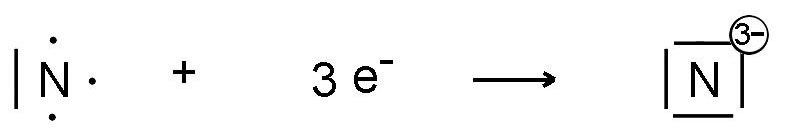 Die Nomenklatur der Anionen ist diejenige, die in den Namen von Verbindungen enthalten ist, z. B. Bromidion, Oxidion, Nitridion.
Ein Atom kann nicht mehr als 3 Elektronen gewinnen, weil die zunehmende negative Ladung die Akquisition eines zusätzlichen Elektrons immer schwieriger macht (Abstoßung zwischen Ladung und e-). Diese Möglichkeit ist daher nur für Azotide (Stickstoffgruppenelemente), Chalkogene und Halogene geeignet.
- indem die Elektronen der letzten Schicht aufgegeben werden:
Die vorletzte Schicht wird die letzte und ist so mit der stabilen Struktur eines Edelgases vervollständigt!
Da die Anzahl der Protonen im Kern gleich bleibt, haben diese Ionen weniger Elektronen als Protonen. Sie werden zu positiven Ionen (Kationen)
Die Nomenklatur der Anionen ist diejenige, die in den Namen von Verbindungen enthalten ist, z. B. Bromidion, Oxidion, Nitridion.
Ein Atom kann nicht mehr als 3 Elektronen gewinnen, weil die zunehmende negative Ladung die Akquisition eines zusätzlichen Elektrons immer schwieriger macht (Abstoßung zwischen Ladung und e-). Diese Möglichkeit ist daher nur für Azotide (Stickstoffgruppenelemente), Chalkogene und Halogene geeignet.
- indem die Elektronen der letzten Schicht aufgegeben werden:
Die vorletzte Schicht wird die letzte und ist so mit der stabilen Struktur eines Edelgases vervollständigt!
Da die Anzahl der Protonen im Kern gleich bleibt, haben diese Ionen weniger Elektronen als Protonen. Sie werden zu positiven Ionen (Kationen)


 Die Nomenklatur Kationen sind die von den Atomen in den Namen von den zusammengesetzten Körpern, z. B. Natriumionen, Bariumionen, Aluminiumionen.
Ein Atom kann nicht mehr als 3 Elektronen verlieren, weil die zunehmende positive Ladung den Verlust eines zusätzlichen Elektrons immer schwieriger macht (Anziehung zwischen + Ladung und und e- ). Diese Möglichkeit ist daher nur für Alkalimetalle, Erdalkalis und Borgruppenelemente gegeben.
Die Nomenklatur Kationen sind die von den Atomen in den Namen von den zusammengesetzten Körpern, z. B. Natriumionen, Bariumionen, Aluminiumionen.
Ein Atom kann nicht mehr als 3 Elektronen verlieren, weil die zunehmende positive Ladung den Verlust eines zusätzlichen Elektrons immer schwieriger macht (Anziehung zwischen + Ladung und und e- ). Diese Möglichkeit ist daher nur für Alkalimetalle, Erdalkalis und Borgruppenelemente gegeben.