





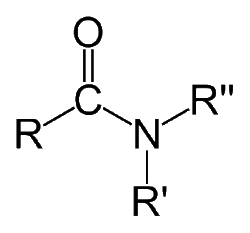
 $R',R''$ = $H$ ou alkyle(amide substituée)
$R',R''$ = $H$ ou alkyle(amide substituée)

- Les ponts H entre molécules d'amides expliquent leurs températures de fusion et d'ébullition élevées :
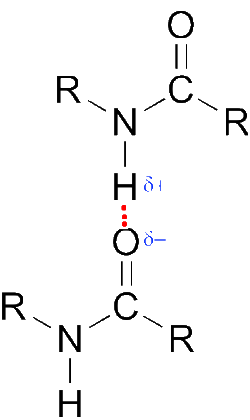 La méthanamide est liquide, alors que l'éthanamide est déjà solide à température normale.
La méthanamide est liquide, alors que l'éthanamide est déjà solide à température normale.
- Les ponts H entre molécules d'amides et molécules d'eau expliquent la solubilité des amides dans l'eau :
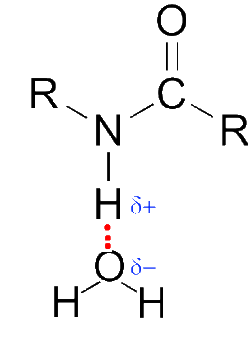 À partir de la heptanamide cependant, le caractère hydrophobe de la chaîne hydrocarbonée l'emporte et la solubilité devient faible, puis nulle.
À partir de la heptanamide cependant, le caractère hydrophobe de la chaîne hydrocarbonée l'emporte et la solubilité devient faible, puis nulle.
1) Réaction avec le carbonate d'ammonium pour former le carboxylate d'ammonium: $2 R-COOH+(NH_4)_2CO_3 \rightarrow 2 R-COO^-NH_4^+ + 2CO_2 + 2 H_2O$ puis chauffage pour former l'amide par déshydratation: 2)$2 R-COO^-NH_4^+ \rightarrow 2 R-CO(NH_2) + 2H_2O$
Réaction violente avec l'ammoniac pour former l'amide et le chlorure d'ammonium:
$2 R-COCl+2NH_3 \rightarrow R-CO(NH_2) + NH_4^+Cl^-$
Le mécanisme procède par attaque nucléophile de l'ammoniac sur le carbone de la fonction chlorure d'acide:

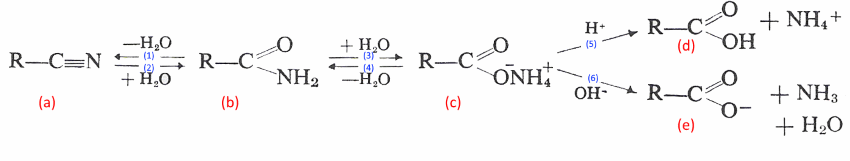
Les amides (b) sont intermédiaires entre nitriles (a) et carboxylates d'ammonium (c) - (1) Déshydratation par $P_2O_5$ - (2) Hydratation par $HCl$ dilué - (3) Déshydratation à chaud - (4) Hydrolyse - par $HCl$ dilué donne le carboxylate d'ammonium (c) qui est ensuite transformé (5) en acide carboxylique (d) - par $NaOH$ dilué donne le carboxylate d'ammonium (c) qui est ensuite transformé (6) en carboxylate (e)
La mésomérie:
 fait apparaître une charge partielle positive sur l'azote. Cette charge retient le doublet de l'azote ce qui réduit fortement la basicité des amides.
fait apparaître une charge partielle positive sur l'azote. Cette charge retient le doublet de l'azote ce qui réduit fortement la basicité des amides.
Nommer les substances finales obtenues à partir des réactifs: - Chlorure de propanoyle et diméthylamine →
- Méthanamide et acide chlorhydrique dilué →
-N-propyl-N-méthyléthanamide et hydroxyde de sodium dilué →