







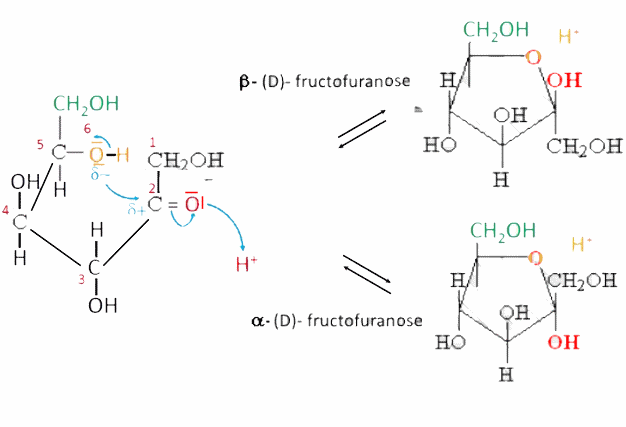
En solution aqueuse, l'attaque nucléophile de l'oxygène de l'avant-dernier groupement hydroxyde sur le carbone du carbonyle qui mène ä la structure $-O-C(OH)-$ est une hémiacétilisation:

- La réaction produit un hétérocycle (un pont $-O-$) - Suivant que le cycle a 5 ou 6 atomes, il est apparenté au furane ou pyrane:

- Un nouvel atome C asymétrique ($C^*$) est formé. - L'énantiomère $\alpha$ a son groupe hydroxyde en-dessous du cycle, c.à .d. de côté opposé au groupement $-CH_2OH$ terminal. - L'énantiomère $\beta$ a son groupe hydroxyde au-dessus du cycle, c.à .d. du même côté que le groupement $-CH_2OH$ terminal.


Les représentations des formes cycliques peuvent varier, celle de droite (forme chaise) du $\beta$-D-glucopyranose est le plus près de la réalité.