







Dans ce cas, le doublet participe à la mésomérie du cycle et y fait apparaître des charges négatives en ortho et para dans les formes contributives: Exemples: Le phénol
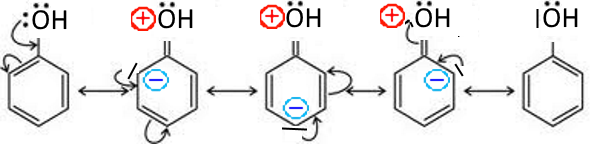
La charge positive ( partielle, moyenne des formes contributives ) de $O$ augmente son pouvoir d'attraction sur le doublet de la liaison $O-H$ tout en facilitant ainsi le départ de $H^+$ ce qui explique l'acidité forte du phénol par rapport aux alcools aliphatiques
L'aniline
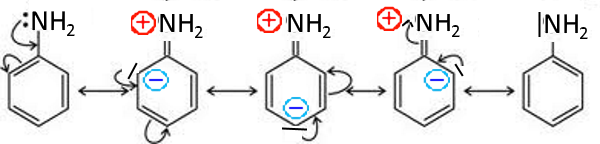
Le doublet de l'azote n'est que peu disponible ce qui explique la basicité faible de l'aniline par rapport aux amines aliphatiques!
Dans ce cas, un doublet du benzène tend à étendre la mésomérie vers cet atome et fait apparaître des charges positives en ortho et para dans les formes contributives: Exemple: L'acide benzoîque
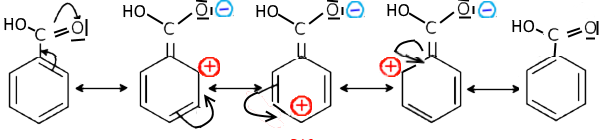
L'augmentation de la densité électronique sur le carbone de la fonction acide carboxylique refoule les électrons de la liaison $O-H$ vers l'hydrogène et gêne ainsi le départ de $H^+$ ce qui explique l'acidité faible par rapport aux acides carboxyliques aliphatiques