






Le pyrrole est un liquide huileux incolore qui se colore en rouge sous l'action des acides ("pyr oleum")

Erich Hückel 1896-1980
D'après Hückel, les systèmes à 4·n+2 électrons disponibles et conjugés ont une mésomérie particulièrement efficace. Le pyrrole possède 2 paires d'électrons π dans ses doubles liaisons et une paire disponible sur l'atome d'azote et vérifie ainsi la règle de Hückel pour n=1.

Une charge partielle négative s'accumule sur le cycle carboné, alors que l'atome d'azote est plutôt chargé positivement. Comparé au furanne où la paire d'électrons est beaucoup plus fortement retenue par la forte électronégativité de l'atome d'oxygène et où donc l'effet mésomère est peu important, le dipôle se trouve renversé:

Substitution électrophile:
Du fait de la mésomérie, comme dans les cas du cycle benzénique activé ( aniline, phénol, chlorobenzène...), les substitutions électrophiles ( nitrations, halogénations, alkylations..) sont faisables sur le noyau pyrrolique.
Basicité:
Du fait de la mésomérie, la paire d'électrons de l'azote est peu disponible pour capter des ions $H^+$, d'où la faible basicité du pyrrole!
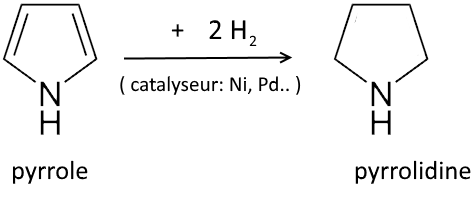
Hydrogénation:
Du fait de la mésomérie, le pyrrole est une molécule très stable (énergie de résonance = 20 kcal/mol). L'hydrogénation est par conséquent difficile:
Le noyau pyrrolique existe dans beaucoup de substances naturelles, par exemple dans:
La proline:

Le tryptophane:

La nicotine:

L'atropine:

La cocaïne:

L'hème, constituant de l'hémoglobine:

Le cytochrome:

La chlorophylle:
