





 Adolphe Wurtz 1817-1884
Adolphe Wurtz 1817-1884
On ajoute dans un ballon sec - une solution d'un halogénoalcane $R-X$ dans un solvant inerte - du sodium $Na$ ou bien du lithium $Li$ métallique La réaction est immédiate: $2R-X+2Na\rightarrow R-R +2NaX$ $2R-X+2Li\rightarrow R-R +2LiX$ Le couplage produit une molécule symétrique!

Dans le ballon se trouve une solution de chloroéthane dans un solvant inerte additionnée de quelques morceaux de lithium Le produit de la réaction est un gaz recueilli dans un gazomètre. Un litre de ce gaz c.n.t.p. est recueilli dans un ballon gonflable et pesé:
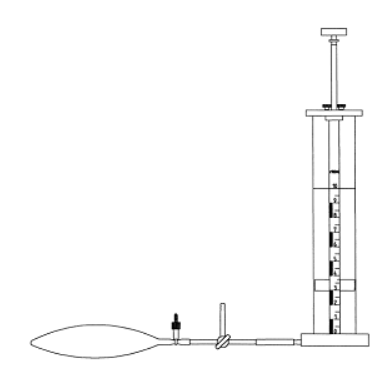
On trouve: c.n.t.p.: $\rho= 2,60 \; \frac{g}{L}$ Calculer la masse molaire du produit et confirmer la réaction de couplage! →
Écrire les produits des réactions des halogénoalcanes suivants avec le sodium: - 2-iodopropane →
- 1,2-dichloroéthane →
- Dichlorocyclopropane →