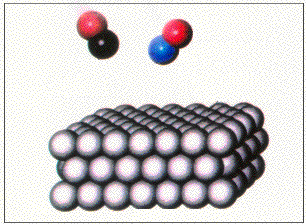
On parle de catalyse hétérogène quand le catalyseur se trouve dans une phase différente de celle des réactifs et produits.

Souvent les réactifs (ici $A$ et $B$) sont adsorbés sur un catalyseur solide ($C$) et s'y combinent pour former le(s) produit(s) ($P$) qui se dégage(nt) par la suite:
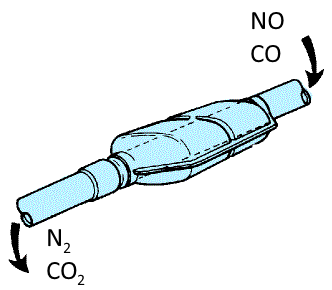
Dans les pots catalytiques des voitures une réaction (entre autres) est la conversion des gaz toxiques monoxyde d'azote et monoxyde de carbone en dioxyde de carbone et (di)azote: $2\;NO$ $+$ $2\;CO$ $\longrightarrow$ $2\;CO_2$ $+$ $N_2$ Cette réaction est accélérée sur un catalyseur solide, le métal rhodium. Le mécanisme paraît être le suivant: