





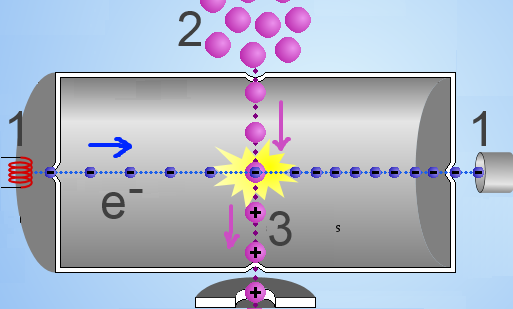
Une tension élevée (1) projette des électrons dans une enceinte où ils heurtent violemment les molécules d'une substance à analyser (2). Il y a extraction d'électrons du corps de la molécule qui se transforme ainsi en ion positif, dit "ion moléculaire" (3), : $AB$ $+$ $e^-$ $\rightarrow$ $AB^+$ $+$ $2e^-$ L'ion moléculaire est souvent instable et se décompose en "fragments moléculaires" (3), dont certains sont chargés positivement: $AB^+$ $\rightarrow$ $A^+$ $+$ $B$ ou $AB^+$ $\rightarrow$ $A$ $+$ $B^+$ Les ions positifs ainsi formés sont accélérés pour être analysés par la suite.
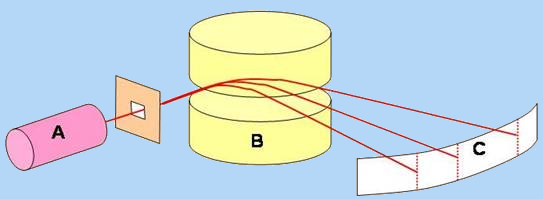
Un champ magnétique B permet de séparer les ions positifs produits en A. Ceux dont le rapport $\frac{masse}{charge}$ est le plus grand seront le moins déviés. Un analyseur C permet de tracer le spectre de masse:
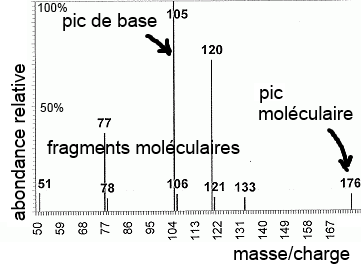
L'ion moléculaire est évidemment le plus lourd, sa charge est égale à +1, donc il est le moins dévié. La spectrométrie de masse permet de déterminer sa masse molaire (pic moléculaire), donc aussi celle de la substance à analyser. La déviation des fragments moléculaires permet de déterminer leurs masse molaires et de deviner ainsi de quels fragments il peut s'agir. Le pic de base correspond au fragment le plus stable (souvent stabilisé par effet inductif ou mésomère). L'abondance relative par rapport au pic de base permet classer les fragments selon leur stabilité.