Recherche:

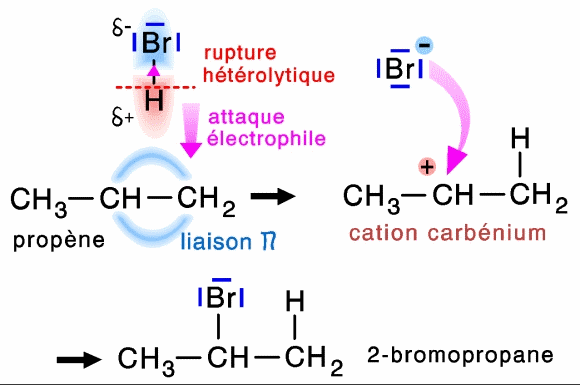
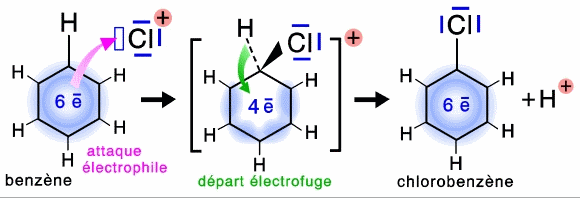
Un électrophile peut être une molécule ou un cation qui possède une lacune électronique (seulement 6 électrons dans la dernière couche d'un de ses atomes).
Un centre nucléophile est une partie d'une molécule ou d'un anion qui possède un doublet électronique qui peut être mis à disposition de l'électrophile pour lui permettre de former une liaison dative.
Dans ce cas, l' électrophilie (importance du caractère électrophile) dépend de plusieurs facteurs:
1) La Charge:
Les réactifs qui ont une ou plusieurs charges positives sur l'atome porteur de la lacune sont meilleurs électrophiles que des réactifs semblables ayant seulement une charge partielle positive ou aucune charge positive sur l'atome en question.
C'est que les charges positives attirent plus fortement le doublet du centre nucléophile! Par ordre décroissant d'électrophilie, on trouve par exemple:
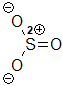 trioxyde de soufre
trioxyde de soufre
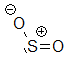 dioxyde de soufre
2) L'Électronégativité:
Les atomes qui sont moins électronégatifs sont moins électrophiles que des atomes semblables dans une même période.
C'est que les atomes moins électronégatifs attirent moins fortement le doublet électronique du centre nucléophile! Par ordre décroissant d'électrophilie, on trouve par exemple:
dioxyde de soufre
2) L'Électronégativité:
Les atomes qui sont moins électronégatifs sont moins électrophiles que des atomes semblables dans une même période.
C'est que les atomes moins électronégatifs attirent moins fortement le doublet électronique du centre nucléophile! Par ordre décroissant d'électrophilie, on trouve par exemple:
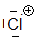 chloronium
chloronium
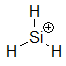 Nous voyons que l'électrophilie décroît de droite à gauche dans une période du tableau périodique: $Cl\gt Si$
3) La Taille de l'atome porteur du doublet:
Les atomes qui sont plus petits sont plus électrophiles que des atomes semblables dans une même famille.
C'est que les atomes plus petits attirent plus fortement le doublet électronique du centre nucléophile (loi de Coulomb)! Par ordre décroissant de d'électrophilie, on trouve par exemple:
Nous voyons que l'électrophilie décroît de droite à gauche dans une période du tableau périodique: $Cl\gt Si$
3) La Taille de l'atome porteur du doublet:
Les atomes qui sont plus petits sont plus électrophiles que des atomes semblables dans une même famille.
C'est que les atomes plus petits attirent plus fortement le doublet électronique du centre nucléophile (loi de Coulomb)! Par ordre décroissant de d'électrophilie, on trouve par exemple:
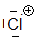 chloronium
chloronium
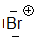 bromonium
Nous voyons que l'électrophilie décroît de haut en bas dans une famille du tableau périodique: $Cl \gt Br$
4) L'Effet inductif des groupes attachés à l'atome porteur de la lacune:
Les groupes à effet I+ diminuent l'électrophilie. En effet, ils pompent les électrons vers la lacune. Ces nouveaux électrons tendent à repousser le doublet électronique du centre nucléophile! L'inverse est vrai pour les groupes à effet I-. Par ordre décroissant d'électrophilie, on trouve par exemple:
bromonium
Nous voyons que l'électrophilie décroît de haut en bas dans une famille du tableau périodique: $Cl \gt Br$
4) L'Effet inductif des groupes attachés à l'atome porteur de la lacune:
Les groupes à effet I+ diminuent l'électrophilie. En effet, ils pompent les électrons vers la lacune. Ces nouveaux électrons tendent à repousser le doublet électronique du centre nucléophile! L'inverse est vrai pour les groupes à effet I-. Par ordre décroissant d'électrophilie, on trouve par exemple:
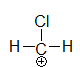 chlorométhylium
chlorométhylium
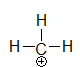 méthylium
méthylium
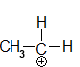 éthylium
éthylium
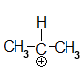 prop-2-ylium
Les groupes méthyle attachés à l'atome C porteur de la lacune exercent un effet $I^+$, le chlore exerce un effet $I^-$
prop-2-ylium
Les groupes méthyle attachés à l'atome C porteur de la lacune exercent un effet $I^+$, le chlore exerce un effet $I^-$

Un électrophile peut être une molécule qui possède une charge partielle positive permanente (molécule polaire) ou temporaire (molécule polarisable). Dans ce cas, il doit en général abandonner une partie de sa molécule à l'attaque.
Dans ce cas, l' électrophilie (importance du caractère électrophile) dépend de plusieurs facteurs:
1) L'importance de la charge partielle: Les réactifs qui ont une charge partielle positive plus importante sont meilleurs électrophiles.
C'est que les charges positives attirent plus fortement le doublet du centre nucléophile! Par ordre décroissant d'électrophilie, on trouve par exemple:
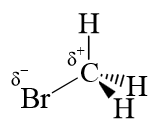
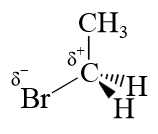 Dans le dernier cas, l'effet $I^+$ du groupe méthyle diminue la charge partielle du carbone.
2)L'importance du groupe sortant:
Moins le groupe sortant est basique, plus il sera stable avec la paire d'électrons qu'il emporte et plus son départ sera facilité!
Par stabilité décroissante: $H_2O \gt OH^-$ et $I^-\gt Br^- \gt Cl^-$
Par ordre décroissant d'électrophilie, on trouvera par exemple dans de nombreuses réactions:
Dans le dernier cas, l'effet $I^+$ du groupe méthyle diminue la charge partielle du carbone.
2)L'importance du groupe sortant:
Moins le groupe sortant est basique, plus il sera stable avec la paire d'électrons qu'il emporte et plus son départ sera facilité!
Par stabilité décroissante: $H_2O \gt OH^-$ et $I^-\gt Br^- \gt Cl^-$
Par ordre décroissant d'électrophilie, on trouvera par exemple dans de nombreuses réactions:
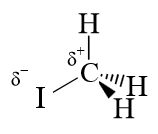 iodomethane
iodomethane
 bromomethane
Nous voyons que la stabilité du groupe sortant l'emporte parfois sur son électronégativité
Notons bien que les critères énumérés en haut ne sont que des indications. Le contexte des réactions (solvant, température, nature du substrat..) jouent parfois un rôle déterminant.
bromomethane
Nous voyons que la stabilité du groupe sortant l'emporte parfois sur son électronégativité
Notons bien que les critères énumérés en haut ne sont que des indications. Le contexte des réactions (solvant, température, nature du substrat..) jouent parfois un rôle déterminant.
Voici des quelques exemples :