







Recherche:
Vers le milieu du 19e siécle, le chimiste Kékulé proposait la structure suivante du benzène $C_6H_6$:

1)
En substituant deux atomes $H$ du benzène par des atomes $Cl$, on ne trouve jamais que trois dichlorobenzènes, alors qu'on aurait dû en trouver quatre:
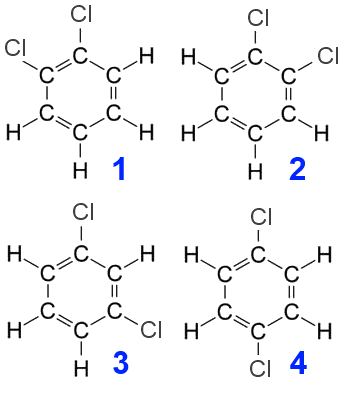 2)
La longueur d'une simple liaison C-C vaut $154\cdot 10^{-12} \;m$, celle d'une double liaison C=C vaut $134\cdot 10^{-12}\;m$ .
Dans le benzène par contre, toutes les liaisons ont la même longueur! $139\cdot 10^{-12}$ m, intermédiaire entre les deux précédentes:
3)
En additionnant une mole de $H_2$ à une mole de benzène, on gagne $120\; kJ$ d'énergie.
Pour hydrogéner trois moles de doubles liaisons C=C, il faudrait donc gagner $360 \;kJ$.
Or en transformant une mole de benzène réel en cyclohexane, on ne gagne en réalité que $208\; kJ$!
2)
La longueur d'une simple liaison C-C vaut $154\cdot 10^{-12} \;m$, celle d'une double liaison C=C vaut $134\cdot 10^{-12}\;m$ .
Dans le benzène par contre, toutes les liaisons ont la même longueur! $139\cdot 10^{-12}$ m, intermédiaire entre les deux précédentes:
3)
En additionnant une mole de $H_2$ à une mole de benzène, on gagne $120\; kJ$ d'énergie.
Pour hydrogéner trois moles de doubles liaisons C=C, il faudrait donc gagner $360 \;kJ$.
Or en transformant une mole de benzène réel en cyclohexane, on ne gagne en réalité que $208\; kJ$!

Il faut admettre que le benzène ne possède ni doubles, ni simples liaisons, mais des liaisons "intermédiaires":
 Cela expliquerait
1) que les structures 1 et 2 sont identiques puisqu'alors dans les deux cas les atomes de chlore seraient portés par des carbones liés identiquement.
2) que toutes les liaisons auraient même longueur
3) que l'énergie reçue par hydrogénation complète du benzène serait différente de ce à quoi on s'attendrait.
Cela expliquerait
1) que les structures 1 et 2 sont identiques puisqu'alors dans les deux cas les atomes de chlore seraient portés par des carbones liés identiquement.
2) que toutes les liaisons auraient même longueur
3) que l'énergie reçue par hydrogénation complète du benzène serait différente de ce à quoi on s'attendrait.

Le benzène réel n'a ni la structure A, ni la structure B, mais une structure intermédiaire difficile à représenter par les structures de Lewis traditionnelles (2 électrons = un trait !). Pour garder la représentation commode de Lewis, on représente tout simplement le benzène par les deux structures de Lewis dont il est l'intermédiaire:
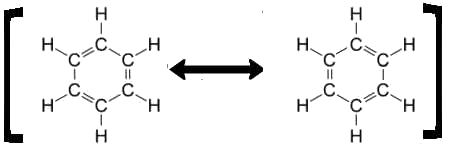
L'image représente une seule molécule intermédiaire entre les deux structures "contributives" qui ne représentent pas des molécules réelles. La double fléche ne représente donc pas un équilibre entre deux molécules mais indique que la seule molécule réelle représentée est un intermédiaire entre ces deux structures contributives.
Un enfant féru de contes de fées n'a jamais vu de rhinocéros. Vous voulez lui expliquer à quoi cela ressemble. Alors vous dites qu'un rhinocéros (qui existe bien) est en quelque sorte un intermédiaire entre une licorne et un dragon (que l'enfant connaît bien, mais qui n'existent pas):

Mésomérie ou résonance désigne le fait qu'une espèce chimique (molécule, ion ou radical) est un intermédiaire entre plusieurs formes contributives imaginaires.