





Le point d'équivalence d'une titration est le point où le nombre de moles du titrant ajouté $n_1$ est tout juste égal au nombre de moles du titré présents au départ $n_2$.
On titre un réactif 1 par un réactif 2: Au p.E. on a: $n_1=n_2$ $c_1 \cdot V_1$ $=$ $c_2 \cdot V_2$ $c_1$ $=$ $\frac{c_2 \cdot V_2}{V_1}$ Connaissant la molarité du réactif titrant $c_2$ et le volume du réactif titré $V_1$, il suffit de détecter le volume du réactif titrant utilisé au p.E. pour connaître la molarité du réactif titré $c_1$.
Au point d'équivalence: $c_1$ $=$ $\frac{c_2 \cdot V_2}{V_1}$
On détecte le point d'équivalence: a) en enregistrant la courbe de titration à l'aide d'un $pH$-mètre. Le saut de $pH$ au p.E. nest détectable avec précision que si lacide et la base sont assez forts et si les dilutions ne sont pas trop poussées. b) par conductimétrie. Avant ou après le p.E. le milieu renferme des ions hydronium ou hydroxyde en excès. Ces ions sont en général plus petits et donc plus mobiles que les ions présents au p.E. et conduisent donc plus facilement le courant électrique. (Transport du courant dans les solutions ioniques = Migration dions): Le p.E. est caractérisé par un minimum de la conductivité électrique. c) par les indicateurs colorés. Nous exigeons dun bon indicateur que son virage se fasse aussi exactement que possible au point équivalent.

La figure représente la courbe de titration dune solution de $10\; mL$ $NaOH$ $0,1\; M$ par une solution de $H Cl$ $0,1\; M$. Les domaines de virage de trois indicateurs colorés sont représentés. Nous voyons que la phénolphtaléine vire (domaine d1) avant quon ait ajouté le volume dacide nécessaire pour atteindre le p.E. $(10\; mL)$, le bleu de thymol après (domaine d2). Lindicateur approprié est ici le tournesol dont le $pKa$ se situe vers 7. Rappelons que le domaine de virage des indicateurs est centré sur la valeur de leur $pKa$ .
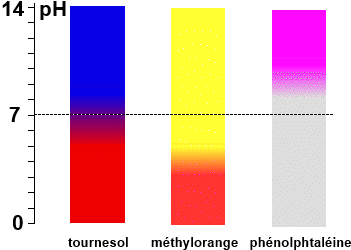
Le $pH$ au p.E. se situe toujours à 7: Tournesol et bleu de bromothymol sont les meilleurs indicateurs.
Au p.E. de la titration des acides faibles par des bases fortes le $pH$ se situe souvent au-dessus de 7 parce quà ce moment le milieu renferme uniquement la base faible correspondante à lacide faible de départ: En principe, il faut choisir lindicateur dont le $pKa$ est le plus proche du $pH$ calculé pour le p.E., mais en pratique, la phénolphtaléine est souvent indiquée.
Au p.E. de la titration des bases faibles par des acides forts le $pH$ se situe souvent en-dessous de 7 parce quà ce moment le milieu renferme uniquement lacide faible correspondant à la base faible de départ: En principe, il faut choisir lindicateur dont le $pKa$ est le plus proche du pH calculé pour le p.E., mais en pratique, le méthylorange est souvent indiqué.