





On mélange $100\; mL$ dacide acétique $0,1\; M$ avec $300\; mL$ dacétate de sodium $0,1\; M$ (tampon acétique bien connu)
a) Etablir pour ce mélange 5 équations entre les molarités à léquilibre :
$[Na^+]$, $[H_3O^+]$, $[CH_3COO^-]$, $[CH_3COOH]$ et $[OH^-]$
(La condition délectroneutralité, deux conditions de conservation de la matière, une condition déquilibre et le produit ionique de leau)
b) Montrer que la résolution de ce système mène à l'équation
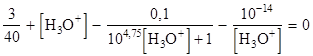 c) Résoudre cette équation en utilisant → ceci .
c) Résoudre cette équation en utilisant → ceci .