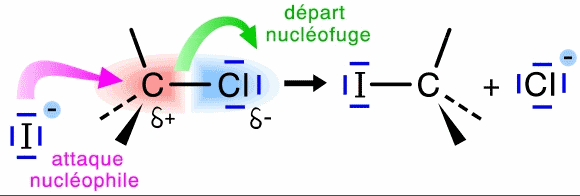
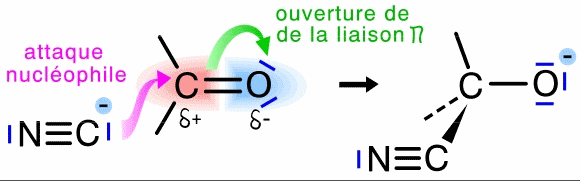
Cliquer dans l'ordre

Un nucléophile est une molécule ou un anion qui possède un doublet électronique non engagé dans une liaison. Un centre électrophile est une partie d'une molécule ou d'un cation qui attire le doublet électronique du nucléophile pour lui permettre de former une liaison dative.
La nucléophilie (importance du caractère nucléophile) dépend de plusieurs facteurs: 1) La charge: Les réactifs qui ont une ou plusieurs charges négatives sur l'atome porteur du doublet sont meilleurs nucléophiles que des réactifs semblables ayant seulement une charge partielle négative ou aucune charge négative sur l'atome en question. C'est que les charges négatives repoussent le doublet et le rendent plus accessible! Par ordre décroissant de nucléophilie, on trouve par exemple:

éthanolate

éthanol
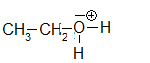
éthyloxonium
2) L'électronégativité: Les atomes qui sont plus électronégatifs sont moins nucléophiles que des atomes semblables dans une même période. C'est que les atomes plus électronégatifs retiennent plus fortement leurs doublets électroniques qui sont ainsi moins disponibles! Par ordre décroissant de nucléophilie, on trouve par exemple:

éthanamine

éthanol

chloroéthane
Nous voyons que la nucléophilie décroît de gauche à droite dans une période du tableau périodique: N > O > Cl 3) La taille de l'atome porteur du doublet: Les atomes qui sont plus gros sont plus nucléophiles que des atomes semblables dans une même famille. C'est que les atomes plus gros retiennent moins fortement leurs doublets électroniques qui se trouvent plus loin du noyau! Par ordre décroissant de nucléophilie, on trouve par exemple:

iodoéthane

bromoéthane

chloroéthane
Nous voyons que la nucléophilie croît de haut en bas dans une famille du tableau périodique: Cl < Br < I 4) L'effet inductif des groupes attachés à l'atome porteur du doublet: Les groupes à effet I+ augmentent la nucléophilie. En effet, ils pompent les électrons vers l'atome porteur du doublet. Ces nouveaux électrons repoussent le doublet et le rendent donc plus accessible. L'inverse est vrai pour les groupes à effet I-. Par ordre décroissant de nucléophilie, on trouve par exemple:

propanamine

éthanamine
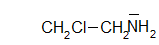
chloroéthanamine
Le groupe propyle exerce un effet I+ plus grand sur l'atome N que le groupe éthyle, le groupe chloroéthyle exerce un effet I- 5) L'effet mésomère d'un système aromatique attaché à l'atome porteur du doublet diminue la nucléophilie. En effet, le doublet est amené à participer à la mésomérie ce qui diminue sa disponibilité. Par ordre décroissant de nucléophilie, on trouve par exemple:

cyclohexanamine

aniline (phénylamine)
Le groupe phényle exerce un effet M- sur l'atome N .
Voici des exemples provenant du site de l'Athénée de Luxembourg → que voici
: