






Un pont électrolytique (qui pourrait être remplacé par une membrane semi-perméable) rempli d'une solution de sulfate de sodium empêche le contact direct entre $Cu^{2+}$ et $Zn$ Si $Cu^{2+}$ et $Zn$ étaient en contact direct, ils réagiraient normalement suivant: $Cu^{2+}$$ +Zn $ $\longrightarrow$ $Cu$$+Zn^{2+}$ Le conducteur électrique permet l'échange d'électrons par voie détournée: $Zn$ $-$ $2e^-$(passent dans le conducteur)$\longrightarrow$ $Zn^{2+}$ $Zn^{2+}$ passe en solution. L'apport de charges positives fait en sorte que ce compartiment se charge positivement! $Cu^{2+}$$+$ $2e^-$(proviennent du conducteur)$\longrightarrow$$ Cu$ $Cu$ se dépose sur l'électrode. La disparition de charges positives fait en sorte que ce compartiment se charge négativement à cause de l'excés d'ions sulfate ! Le pont électrolytique (ou la membrane semi-perméable) compense les charges: - des ions $Zn^{2+}$ migrent vers le compartiment de droite - des ions sulfate migrent vers le compartiment de gauche Voir la vidéo: → Pile Cu/Zn
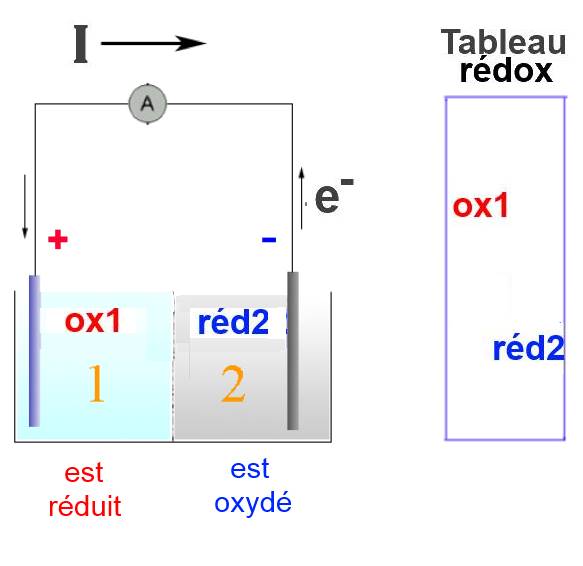
L'oxydant 1 est assez fort pour arracher des électrons au réducteur 2. Il ne peut cependant pas réagir avec lui à cause de la paroi semi-perméable ou du pont électrolytique qui les séparent. Alors
L'échange d'électrons normal se fait par l'intermédiaire du circuit extérieur
Dans le compartiment 2, le réducteur 2 cède des électrons au circuit extérieur: Il est oxydé. Dans le compartiment 1, l'oxydant 1 prend des électrons au circuit extérieur: Il est réduit.
Dans le circuit extérieur, les électrons circulent du réducteur 2 le plus fort vers l'oxydant 1 le plus fort.
Il se produit ainsi un courant électrique d'intensité I dont le sens (sens conventionnel de la physique) est opposé au sens de déplacement des électrons. I va toujours dans le circuit extérieur du pôle positif au pôle négatif.
Le pôle positif de la pile est donc du côté de l'oxydant 1 le plus fort et le pôle négatif du côté du réducteur 2 le plus fort.
Les pertes ou gains de charge dans les deux compartiments 1 et 2 sont compensées par la migration d'anions ou de cations à travers la membrane semi-perméable ou le pont électrolytique.