







Recherche:
Dans l'ion hydronium (hydroxonium) $H_3O^+$ l'atome O forme 3 liaisons avec des atomes H.
Le modèle simple de la liaison covalente de Lewis ( autant de liaisons covalentes que d'électrons célibataires ) doit être élargi pour tenir compte de ce genre d'ions:
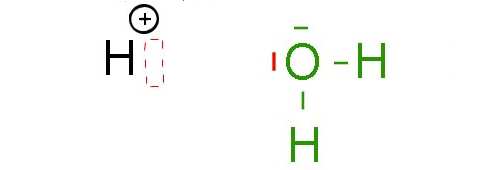 Voici un ion hydrogène et une molécule d'eau.
L'ion hydrogène a de la place pour deux électrons sur sa dernière couche. En effet, la dernière couche de l'ion $H^+$ est vide, mais peut accomoder 2 électrons au maximum. On dit que l'ion $H^+$ possède une lacune électronique
Par contre, l'atome d'oxygène de la molécule d'eau possède (au moins) un doublet électronique sur sa dernière couche. Le "deal" est maintenant le suivant:
Voici un ion hydrogène et une molécule d'eau.
L'ion hydrogène a de la place pour deux électrons sur sa dernière couche. En effet, la dernière couche de l'ion $H^+$ est vide, mais peut accomoder 2 électrons au maximum. On dit que l'ion $H^+$ possède une lacune électronique
Par contre, l'atome d'oxygène de la molécule d'eau possède (au moins) un doublet électronique sur sa dernière couche. Le "deal" est maintenant le suivant:
 En mettant en commun avec l'atome $H$ les deux électrons du doublet, $O$ acquiert le même octet que le gaz noble néon et $H$ acquiert la structure stable de l'hélium!
En mettant en commun avec l'atome $H$ les deux électrons du doublet, $O$ acquiert le même octet que le gaz noble néon et $H$ acquiert la structure stable de l'hélium!
 Il faut quand-même bien se rendre compte, qu'en mettant en commun deux électrons provenant de l'atome O seul, celui-ci perd en moyenne un électron, alors que H en gagne un ce qui fait que O, neutre au début acquiert une charge positive alors que H, chargé positivement au début devient neutre:
Il faut quand-même bien se rendre compte, qu'en mettant en commun deux électrons provenant de l'atome O seul, celui-ci perd en moyenne un électron, alors que H en gagne un ce qui fait que O, neutre au début acquiert une charge positive alors que H, chargé positivement au début devient neutre:

Une liaison dative peut se former entre une espèce chimique possédant une lacune électronique et une espèce possédant un doublet électronique. La première espèce gagne en moyenne un électron et sa charge diminue ainsi d'une unité, la deuxième perd un électron et sa charge augmente d'une unité
Voici différents cas de lacunes:
- L'ion hydrogène, par exemple:
 - Les composés des terreux (troisième famille du tableau périodique): $B$, $Al$, ..., par exemple:
- Les composés des terreux (troisième famille du tableau périodique): $B$, $Al$, ..., par exemple:
 - Les atomes des sulfurides (sixième colonne du tableau périodique): $O$, $S$,.... après réarrangement de leurs électrons extérieurs, par exemple:
- Les atomes des sulfurides (sixième colonne du tableau périodique): $O$, $S$,.... après réarrangement de leurs électrons extérieurs, par exemple:
