







Recherche:
Le modèle de Lewis est basé sur la règle de l'octet et il s'applique souvent à molécules simples ne faisant pas intervenir d'éléments de transition, par exemple:
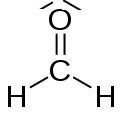 Ce modèle s'applique aussi à des ions polyatomiques simples, par exemple:
Ce modèle s'applique aussi à des ions polyatomiques simples, par exemple:
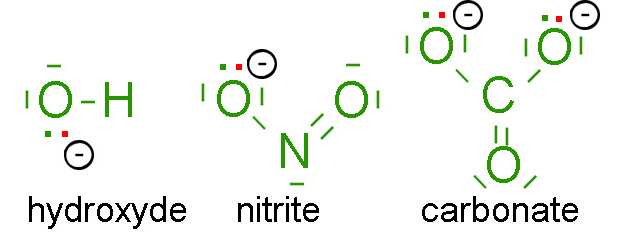 En vert sont représentés les électrons extérieurs des atomes neutres, en rouge les électrons supplémentaires qui déterminent leurs charges.
En vert sont représentés les électrons extérieurs des atomes neutres, en rouge les électrons supplémentaires qui déterminent leurs charges.
Les atomes forment autant de liaisons covalentes qu'il leur reste des électrons non appariés

Pour former la molécule d'eau, l'atome O peut mettre en oeuvre deux électrons non appariés, il forme donc deux liaisons covalentes, alors que dans l'ion hydroxyde, il lui reste un seul électron non apparié pour former une liaison covalente!