







Recherche:
Les atomes métalliques retiennent très faiblement leurs électrons extérieurs. Dans un métal ceux-ci sont libres de se déplacer entre les "troncs" ioniques restants (= le noyau et les électrons intérieurs, le tout positivement chargé) des atomes et forment une sorte de "gaz électronique". Ils assurent ainsi la cohésion de l'ensemble:
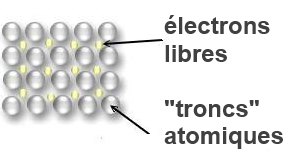
La mobilité des électrons extérieurs explique:
Les propriétés des métaux: - conductivité électrique élevée - conductivité thermique élevée - malléabilité (ils se laissent déformer) - ductilité élevée (ils se laissent étirer) - éclat métallique