







Recherche:
Que se passe-t-il quand deux atomes de chlore isolés sont mis en contact?
 En mettant ensemble leurs électrons non appariés, chacun gagne un octet parfait:
En mettant ensemble leurs électrons non appariés, chacun gagne un octet parfait:
 D'après Lewis, la paire commune d'électrons se représente par un trait:
D'après Lewis, la paire commune d'électrons se représente par un trait:
 On a l'habitude de tracer horizontalement le doublet représentant les deux électrons mis en commun et de l'appeler "liaison covalente":
On a l'habitude de tracer horizontalement le doublet représentant les deux électrons mis en commun et de l'appeler "liaison covalente":
 Il s'est formé une molécule Cl2.
Aucun autre atome de chlore ne peut plus s'y attacher.
Le corps simple (di)chlore est ainsi formé uniquement de molécules Cl2
Il s'est formé une molécule Cl2.
Aucun autre atome de chlore ne peut plus s'y attacher.
Le corps simple (di)chlore est ainsi formé uniquement de molécules Cl2
Que se passe-t-il quand on met en contact en contact des atomes d'oxygène et d'hydrogène?
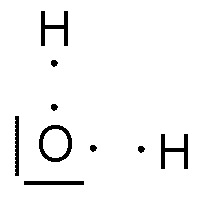
Pour gagner un octet complet, l'atome d'oxygène a besoin de deux atomes d'hydrogène:

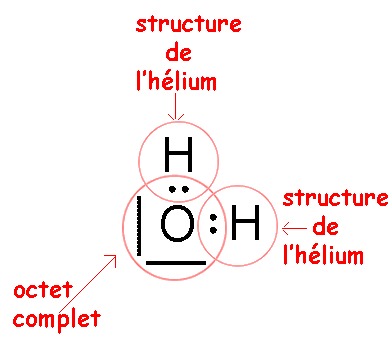 Chaque atome d'hydrogène gagne ainsi la structure stable de l'hélium!
Les paires d'électrons peuvent être représentées par des traits:
Chaque atome d'hydrogène gagne ainsi la structure stable de l'hélium!
Les paires d'électrons peuvent être représentées par des traits:
 Ces traits sont avantageusement tracés d'un atome vers l'autre pour marquer deux "liaisons covalentes".
Ces traits sont avantageusement tracés d'un atome vers l'autre pour marquer deux "liaisons covalentes".
 La molécule d'eau est ainsi constituée.
La molécule d'eau est ainsi constituée.
Voici la formation de la molécule d'ammoniac:

La mise en commun de plusieurs paires d'électrons mème à des liaisons multiples comme dans le cas du
(di)oxygène (liaison double):
 ou encore du (di)azote (liaison triple):
ou encore du (di)azote (liaison triple):
