







Recherche:
Tous les atomes ont tendance à se stabiliser en prenant la structure stable des gaz nobles.
Ceci peut se faire par exemple
- en gagnant un ou plusieurs électrons pour compléter l'octet de la dernière couche :

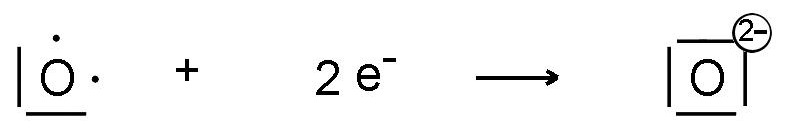
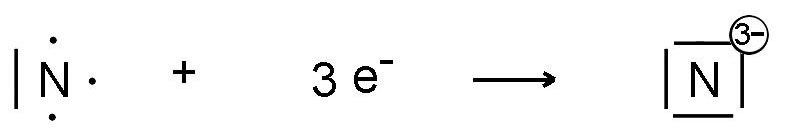 La nomenclature des anions est celle figurant dans les noms des corps composés, p.ex: ion bromure, ion oxyde, ion nitrure.
Un atome ne peut pas gagner plus de 3 électrons, parce que la charge négative croissante rend l'acquisition d'un électron supplémentaire de plus en plus difficile (répulsion entre charge - et -). Cette possibilité convient donc uniquement pour les azotides, sulfurides et halogènes.
- en abandonnant les électrons de la dernière couche:
L'avant-dernière couche deviendra la dernière et elle sera complète avec la structure stable d'un gaz noble!
Comme le nombre de protons dans le noyau reste le même, ces ions auront alors moins d'électrons que de protons. Ils se transformeront en ions positifs (cations), par exemple
La nomenclature des anions est celle figurant dans les noms des corps composés, p.ex: ion bromure, ion oxyde, ion nitrure.
Un atome ne peut pas gagner plus de 3 électrons, parce que la charge négative croissante rend l'acquisition d'un électron supplémentaire de plus en plus difficile (répulsion entre charge - et -). Cette possibilité convient donc uniquement pour les azotides, sulfurides et halogènes.
- en abandonnant les électrons de la dernière couche:
L'avant-dernière couche deviendra la dernière et elle sera complète avec la structure stable d'un gaz noble!
Comme le nombre de protons dans le noyau reste le même, ces ions auront alors moins d'électrons que de protons. Ils se transformeront en ions positifs (cations), par exemple


 La nomenclature des cations est celle des atomes est celle figurant dans les noms des corps composés, p.ex: ion sodium, ion baryum, ion aluminium.
Un atome ne peut pas perdre plus de 3 électrons, parce que la charge positive croissante rend la perte d'un électron supplémentaire de plus en plus difficile (attraction entre charge + et -). Cette possibilité convient donc uniquement pour les alcalins, alcalino-terreux et terreux.
La nomenclature des cations est celle des atomes est celle figurant dans les noms des corps composés, p.ex: ion sodium, ion baryum, ion aluminium.
Un atome ne peut pas perdre plus de 3 électrons, parce que la charge positive croissante rend la perte d'un électron supplémentaire de plus en plus difficile (attraction entre charge + et -). Cette possibilité convient donc uniquement pour les alcalins, alcalino-terreux et terreux.