







L'ion permanganate (violet) possède la formule $MnO_4^- $. Calculer le nombre d'oxydation du manganèse!
Soit x le nombre d'oxydation du manganèse: $x$ $+$ $4(-2)$ $=$ $-1$, donc $x$ $=$ $7$
L'ion manganate (vert) possède la formule $MnO_4^{2-} $. Calculer le nombre d'oxydation du manganèse!
Soit x le nombre d'oxydation du manganèse: $x$ $+$ $4(-2)$ $=$ $-2$, donc $x$ $=$ $6$
L'oxyde et hydroxyde mixte de manganèse (brun) possède la formule $MnO(OH)_2 $. Calculer le nombre d'oxydation du manganèse!
$x$ $+$ $(-2)$ $+$ $2(-2+1)$ $=$ $0$, donc $x$ $=$ $4$
Que s'est-il passé avec le manganèse pendant cette réaction?
Le manganèse a été réduit, donc il a gagné des électrons!
Calculer le nombre d'oxydation des atomes de carbone colorés dans le glucose et l'acide gluconique formé!
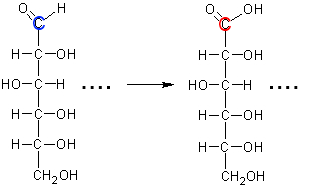
On fait comme si l'atome plus électronégatif dans chaque liaison possédait tous les électrons de cette liaison:
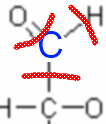 Ainsi le carbone "possède" ici 3 électrons dans la dernière couche, avec 4 il est neutre, donc sa charge fictive (nombre d'oxydation) est +1
Ainsi le carbone "possède" ici 3 électrons dans la dernière couche, avec 4 il est neutre, donc sa charge fictive (nombre d'oxydation) est +1
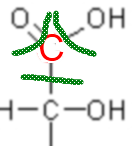
Ainsi le carbone "possède" ici 1 électron dans la dernière couche, avec 4 il est neutre, donc sa charge fictive (nombre d'oxydation) est +3
Que s'est-il passé avec ce carbone pendant cette réaction?
Le carbone a été oxydé, donc il a perdu des électrons.